FDA繼續專注IMDRF決定退出GHWPFDA的擔憂包括領導層不夠多元化或不代表全球視角、監管機構和行業在GHWP中的參與不平衡,以及文件的創建、審查和最終確定缺乏透明度。
FDA計劃重新集中其人員和資源,主要與IMDRF合作。FDA將在2024年主持IMDRF,Shuren在信中邀請徐景和參加明年3月份的IMDRF會議,繼續協調兩個組織之間的討論。
不限 2024 2023 2022 2021 2020 2019 2018 2017 2016 2015 2014 2013 2012 2011 2010 2009 2008 2007 2006

FDA計劃重新集中其人員和資源,主要與IMDRF合作。FDA將在2024年主持IMDRF,Shuren在信中邀請徐景和參加明年3月份的IMDRF會議,繼續協調兩個組織之間的討論。

該公司曾于2022年9月推出了Masimo W1?醫療級手表,這是市場上第一款為消費者提供準確、持續健康數據的可穿戴設備。該產品可以提供持續的健康數據,如氧含量、補水指數、脈搏、心臟和呼吸頻率等指標。FDA的這次批準讓Masimo W1?手表能適用于更廣泛的醫療用途或病癥。

醫療技術的發展,各類醫療器械的應用極大地提升了人類對抗疾病的能力,診斷技術的提高也讓更多疾病可以被盡早發現并應對。其中,IVD(In Vitro Diagnostic)技術引起了廣泛關注,IVD包括體外診斷試劑及儀器,從屬于醫療器械行業。

雙方將在數字化管理服務升級、金融支付數字化服務升級、業務智能服務升級、IT研發智能化服務升級、“+互聯網”創新增長、市場合作探索六大方向開展合作,全方位開展人才交流和技術合作,以期通過數字化技術打造聯合解決方案及產品。
Masimo W1?將其MW1-1傳感器、硬件和軟件模塊脈搏血氧飽和度技術集成到單個可穿戴設備中。Masimo W1?手表包括光學傳感器和心電圖電極片,可以檢測生理信號。Masimo表示,MW1使用該公司專有的信號處理算法處理這些信號,以輸出“來自心電圖的高分辨率SpO2、PR、灌注指數(Perfusion Index,Pi)和心率”。來自模塊的連續數據能夠實時顯示在Masimo W1?手表觸摸屏上,并通過以紅色顯示SpO2和PR值來幫助識別低氧飽和度、高脈搏率或低脈搏率。

美國食品藥品監督管理局(FDA)負責監管和批準醫療器械,確保其安全性和有效性。同時中國制造商為了在美國市場順利地銷售其器械,注冊是制造商必須完成的一項程序。
又一家采用科創板第五套上市標準的IPO項目宣布終止。12月25日,上交所發布公告表示,因北京華脈泰科醫療器械股份有限公司(簡稱“華脈泰科”)及其保薦人撤回發行上市申請,終止其發行上市審核。華脈泰科于2022年底上市申請獲受理,3月底回復首輪問詢,此后審核就處于停滯狀態,直到如今撤回。
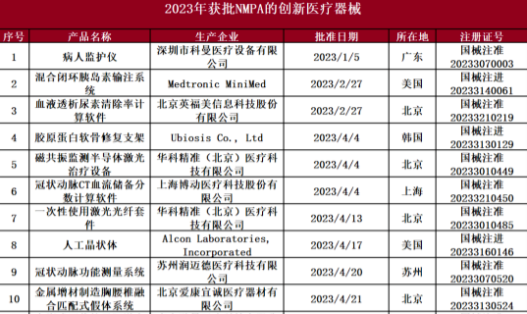
2023年獲批的56款創新醫療器械中,包含了16款心血管相關器械,3款眼科器械,8款影像類器械,10款手術機器人器械,4款骨科植入類器械,以及15款其他創新醫療器械


已有780次查看

已有696次查看
已有717次查看
已有695次查看

已有708次查看
已有813次查看

已有712次查看
已有679次查看
已有685次查看

已有677次查看





