關于印發廣東省加速消除宮頸癌行動計劃(2023—2030年)的通知進一步完善宮頸癌防治服務體系,提高綜合防治能力,構建社會支持環境,努力遏制宮頸癌發病率、死亡率上升趨勢,減輕宮頸癌社會疾病負擔。
各地級以上市衛生健康局(委)、教育局、民政局、財政局、市場監管局、醫保局、中醫藥局、疾控主管部門、總工會、婦聯:現將《廣東省加速消除宮頸癌行動計劃(2023—2030年)》印發給你們,請結合實際,認真貫徹執行。
不限 NMPA 廣東省 江蘇省 浙江省 上海市 北京市 安徽省 河北省 山西省 吉林省 遼寧省 黑龍江省 陜西省 甘肅省 青海省 山東省 福建省 臺灣省 河南省 湖北省 湖南省 江西省 海南省 四川省 貴州省 云南省 天津市 重慶市
不限 2024 2023 2022 2021 2020 2019 2018 2017 2016 2015 2014 2013 2012 2011 2010 2009 2008 2007 2006

各地級以上市衛生健康局(委)、教育局、民政局、財政局、市場監管局、醫保局、中醫藥局、疾控主管部門、總工會、婦聯:現將《廣東省加速消除宮頸癌行動計劃(2023—2030年)》印發給你們,請結合實際,認真貫徹執行。
根據《廣東省藥品監督管理局辦公室關于印發廣東省第二類醫療器械注冊質量管理體系核查工作程序并明確有關工作要求的通知》(粵藥監辦許〔2022〕133號)第二十三條規定,2022年5月份起。
?

保證醫療器械質量安全,保障人體健康和生命安全,促進醫療器械產業發展,根據《醫療器械監督管理條例》(國務院令第739號)、《醫療器械注冊與備案管理辦法》(國家市場監督管理總局令第47號)、《體外診斷試劑注冊與備案管理辦法》(國家市場監督管理總局令第48號)、《醫療器械生產監督管理辦法》(國家市場監督管理總局令第53號),結合我省實際,制定本規定。

根據《醫療器械監督管理條例》《醫療器械注冊與備案管理辦法》《體外診斷試劑注冊與備案管理辦法》等文件要求,有關醫療器械檢驗工作指引如下:
一、注冊自檢工作要求
二、委托檢驗報告要求
三、醫療器械檢驗機構資質要求

一、辦理條件
二、申請材料
三、申請方式
四、辦理程序
五、辦理結果

一、省內申辦者報告醫療器械臨床試驗嚴重不良事件時,可登錄廣東省政務服務網,在已完成備案的醫療器械臨床試驗項目中,選擇相應“報告”選項,在線填寫格式化表格內容,同時上傳蓋章版《醫療器械/體外診斷試劑臨床試驗嚴重不良事件報告表》掃描件,確認無誤并勾選法律聲明后提交,即完成報告。
二、省內申辦者報告醫療器械臨床試驗終止/完成進展情況時,可登錄廣東省政務服務網,在已完成備案的醫療器械臨床試驗項目中,選擇相應“報告”選項,上傳蓋章版情況說明掃描件,確認無誤并勾選法律聲明后提交,即完成報告。
三、省外申辦者報告醫療器械臨床試驗嚴重不良事件的,仍通過線下渠道寄送加蓋公章的紙質報告表,

對產品分類明確、臨床評價證據充分的,技術審評時可僅對產品檢驗報告采納強制性標準的完整性、試劑類產品適用的國家標準品檢測情況進行審查,技術審評時限不超過5個工作日。對產品分類不明確或臨床評價證據不充分的,應按照正常程序開展技術審評。

全省醫療器械注冊人、備案人、受托生產企業應按照《醫療器械生產監督管理辦法》有關要求,認真填寫相關信息,上傳相關材料,并對上報材料的合法、真實、準確、完整和可追溯負責。在系統使用過程中如遇系統操作和技術問題,可致電(020-37886123)或加入QQ群(719256878)進行咨詢,相關政策問題可聯系省藥品監管局醫療器械監管處。


已有777次查看

已有690次查看
已有713次查看
已有691次查看

已有704次查看
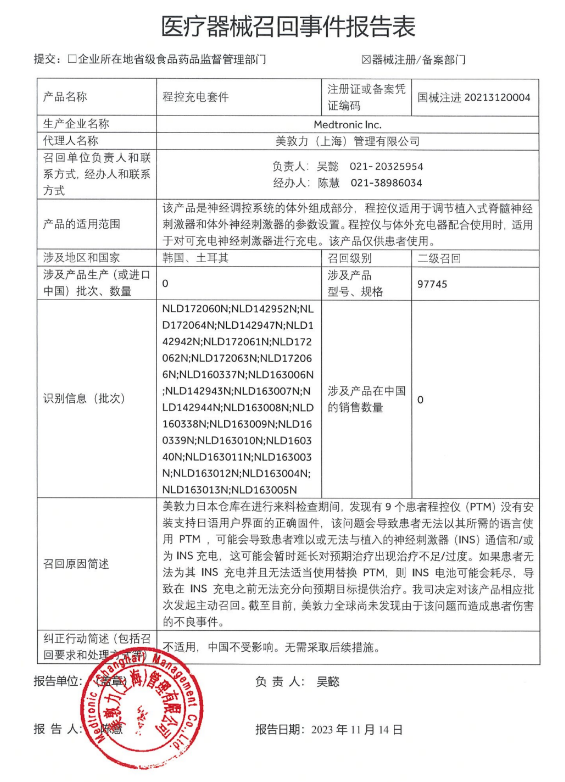
已有808次查看

已有709次查看
已有674次查看
已有679次查看

已有674次查看





