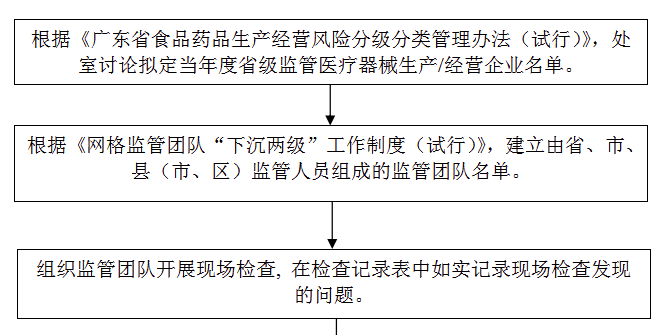
省級重點監管醫療器械日常監督檢查工作流程圖根據《廣東省食品藥品生產經營風險分級分類管理辦法(試行)》,處室討論擬定當年度省級監管醫療器械生產/經營企業名單。
根據《網格監管團隊“下沉兩級”工作制度(試行)》,建立由省、市縣(市、區) 監管人員組成的監管團隊名單。
組織監管團隊開展現場檢查,在檢查記錄表中如實記錄現場檢查發現的問題。
不限 NMPA 廣東省 江蘇省 浙江省 上海市 北京市 安徽省 河北省 山西省 吉林省 遼寧省 黑龍江省 陜西省 甘肅省 青海省 山東省 福建省 臺灣省 河南省 湖北省 湖南省 江西省 海南省 四川省 貴州省 云南省 天津市 重慶市
不限 2024 2023 2022 2021 2020 2019 2018 2017 2016 2015 2014 2013 2012 2011 2010 2009 2008 2007 2006
根據《網格監管團隊“下沉兩級”工作制度(試行)》,建立由省、市縣(市、區) 監管人員組成的監管團隊名單。
組織監管團隊開展現場檢查,在檢查記錄表中如實記錄現場檢查發現的問題。
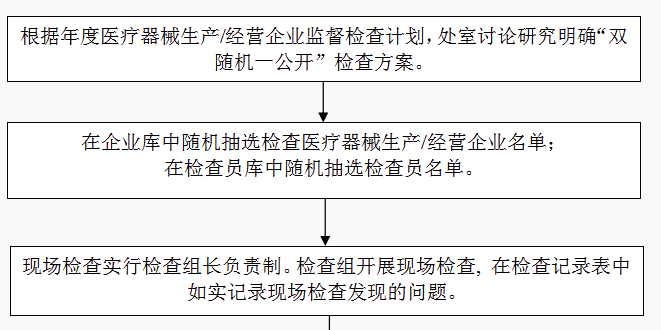
檢查結束時向企業通報檢查情況,并由企業負責人在檢查記錄表上簽字確認。檢查組撰寫檢查報告,檢查報告如實反應檢查全部真實情況處室匯總整理檢查記錄和檢查報告,討論研究檢查結果處理。

為貫徹落實《國務院關于改革藥品醫療器械審評審批制度的意見》(國發〔2015〕44號)以及國務院有關行政審批制度改革精神,進一步加強醫療器械注冊管理,切實提高審評審批效率,經國家食品藥品監督管理總局局務會議研究決定,將下列由國家食品藥品監督管理總局作出的醫療器械行政審批決定,調整為由國家食品藥品監督管理總局醫療器械技術審評中心以國家食品藥品監督管理總局名義作出:

對保障人體健康和生命安全的技術要求,應當制定為醫療器械強制性國家標準和強制性行業標準。對滿足基礎通用、與強制性標準配套、對醫療器械產業起引領作用等需要的技術要求,可以制定為醫療器械推薦性國家標準和推薦性行業標準。

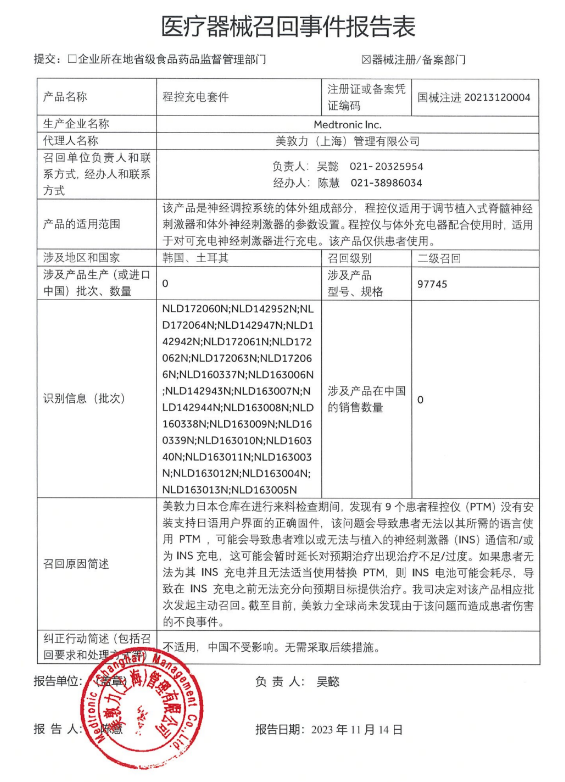
本辦法所稱醫療器械召回,是指醫療器械生產企業按照規定的程序對其已上市銷售的某一類別、型號或者批次的存在缺陷的醫療器械產品,采取警示、檢查、修理、重新標簽、修改并完善說明書、軟件更新、替換、收回、銷毀等方式進行處理的行為。


已有780次查看

已有696次查看
已有717次查看
已有695次查看

已有708次查看
已有813次查看

已有712次查看
已有679次查看
已有685次查看

已有677次查看





