國內首個!國家技術標準創新基地(醫療器械)在高區成立國家技術標準創新基地是標準化試點示范的一種形式,是促進創新成果轉化為技術標準的服務平臺,是以標準化助推創新技術和產品市場化、產業化和國際化的孵化器。
同時,創新基地加大工作創新和機制創新,加強與稀土、化工新材料等創新基地合作,探索原創性醫療器械原材料科研成果轉化為標準,為醫療器械上下游產業鏈融合發展奠定了堅實基礎。
不限 2024 2023 2022 2021 2020 2019 2018 2017 2016 2015 2014 2013 2012 2011 2010 2009 2008 2007 2006

同時,創新基地加大工作創新和機制創新,加強與稀土、化工新材料等創新基地合作,探索原創性醫療器械原材料科研成果轉化為標準,為醫療器械上下游產業鏈融合發展奠定了堅實基礎。

此次集采的兩類耗材中,輸注泵市場較為成熟,此前已在福建、河南、山西、河北等地開展過集采。其中,河南省鎮痛泵類耗材集采中選產品平均降幅83.6%,最高降幅達90.5%。
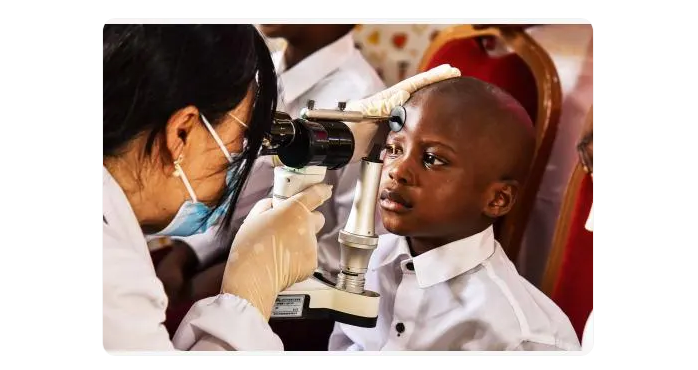
面對日趨內卷的國內存量市場和因生育率下降而受限的增量市場,不少中國AI醫療診斷行業企業開始瞄向非洲、拉美和東南亞等海外市場。然而,盡管一些國產器械在診斷的靈敏度上已達到全球領先水平,但無論是參與國際采購的程度還是在欠發達地區的滲透度,都依然偏低。

最終財政部判定,北京中研海康科技有限公司投訴事項1、2成立(其所投產品為國產產品,符合招標文件要求,本項目評審錯誤),并責令采購人重新開展采購活動,原中標結果一并被作廢。在參與招投標過程中遭遇“小插曲”不奇怪,但是把投標產品國產、進口身份弄錯的確實少見,好在最后供應商通過質疑投訴等手段為自己找回了公道。

作為一家新生代創新醫療器械企業,領博生物能夠成功完成大額融資,充分說明了資本市場對于其團隊以及所處細分賽道的高度認可與看好。此次A輪融資資金,將主要用于公司的生物型人工血管的注冊性臨床試驗,同時持續推進公司其他管線的研發和進一步完善公司技術成果轉化平臺的建設。

對抽檢中發現的上述不符合標準規定產品,國家藥品監督管理局已要求企業所在地省級藥品監督管理部門按照《醫療器械監督管理條例》《醫療器械生產監督管理辦法》和《醫療器械召回管理辦法》等要求,及時作出行政處理決定并向社會公布。省級藥品監督管理部門要督促企業對抽檢不符合標準規定的產品進行風險評估,根據醫療器械缺陷的嚴重程度確定召回級別,主動召回產品并公開召回信息;督促企業盡快查明產品不合格原因,制定整改措施并按期整改到位。

我們需要了解什么是三類醫療器械。根據國家食品藥品監督管理總局(CFDA)的規定,三類醫療器械是指具有較高風險,需要嚴格控制管理以保證其安全有效的醫療器械。例如植入式心臟起搏器、人工關節、血管支架等都屬于三類醫療器械。

基于在全國最早開展醫工交叉研究的深厚積淀,健康與康復科學研究所注重發揮黨支部戰斗堡壘作用,團結帶領全所博士研究生投身產教融合,研發的運動功能評估系統、監測儀等成果已應用于臨床,服務數以萬計的患者。
“在科技飛速發展的今天,如何將理論學習與科學研究相結合,是我們一直思考的問題。幾年來,我們組織帶領研究所的學子深入行業一線,讓大家深刻感受中國醫療器械行業的飛速發展。”健康與康復科學研究所副所長黃子罡說。


已有780次查看

已有696次查看
已有717次查看
已有695次查看

已有708次查看
已有813次查看

已有712次查看
已有679次查看
已有685次查看

已有677次查看





