發布時間:2023-12-25 來源:Qarad;MDCG 作者:

2023年12月19日,醫療器械協調小組(the Medical Device Coordination Group,MDCG)發布了更新版的常見問題解釋文件MDCG 2021-27: Questions and Answers on Articles 13 & 14 of Regulation (EU) 2017/745 and Regulation (EU) 【Rev.1】(針對MDR第13和第14條及歐盟法規的問答)(原文下載地址:https://health.ec.europa.eu/document/download/82d9adbc-dbf0-40d4-93ed-ade673c8232a_en?filename=mdcg_2021-27_en.pdf)
本次更新的內容包括:

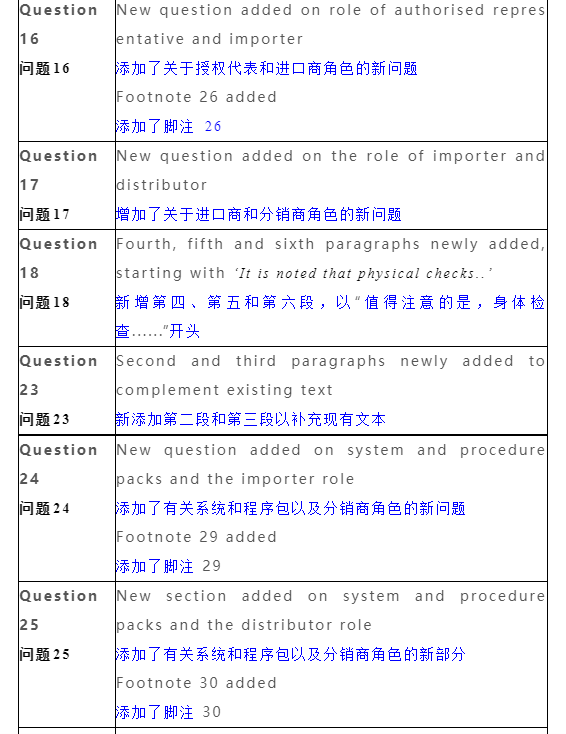

具體變化內容包括:
進口商應始終考慮提供器械最小可銷售包裝(即制造商確定的最終用戶可以購買的最小包裝)的隨附文件,以確保最終用戶了解進口商的詳細信息。如果存在影響器械符合一般安全和性能要求的風險,進口商可以與制造商合作,對于由于其尺寸或配置而在多個盒子中交付的器械,如果產品是提供給單個用戶或機構的情況下,則可以一次性提供隨附文檔,而不是在每個單獨的包裝內提供隨附文檔。
盡管履行服務提供商(Fulfilment Service Providers,FSP)不被定義為經濟運營商,因此不需要履行經濟運營商的義務,如果他們開展的活動也符合 MDR/IVDR 中進口商或分銷商的定義,則條例第 13 條和第 14 條中概述的相關角色和義務確實適用。
同一自然人或法人可以是特定器械的授權代表和進口商,但自然人或法人不能履行單個器械的進口商和分銷商的角色,因為分銷商是“供應鏈中的任何自然人或法人,而不是制造商或進口商,使得產品在市場上流通并最終投入使用。”
關于進口商和分銷商的驗證義務要求,文件指出:物理檢查是確保器械合規性、檢測不合規情況和防止此類不合規器械在市場上銷售的重要工具。在特殊和合理的情況下,如果無法在不損害包裝完整性和器械合規性的情況下,進行此類檢查驗證應基于文件審查。為此,制造商和/或進口商應允許分銷商根據要求獲取歐盟符合性聲明。重要的是,進口商和分銷商可以向主管當局證明他們已通過內部記錄或程序執行了這些驗證檢查,并在適用時考慮到國家規定。
對于由來自第三國制造商的一個或多個帶有CE標志的單個器械組成的系統或程序包(System or Procedure Packs,SPP),在歐盟設立的SSP包生產商(SSP Pack Producer,SSPP)將被視為單個器械的進口商。然而,如果SSP已投放歐盟市場,則SSPP將被視為經銷商。
最后,根據租賃公司在投放市場或提供器械方面開展的具體活動,租賃公司可能被視為進口商或分銷商。如果租賃公司的活動屬于進口商或分銷商的活動范圍,則相關義務將適用于租賃公司。如果租賃公司根本不是供應鏈的一部分(即不開展任何與首次投放市場或提供器械有關的活動),則不應將其視為進口商或經銷商。
Source: Qarad;MDCG





