發布時間:2023-11-30 來源:天之恒 作者:
官方機構/監管當局:Central Drugs Standard Control Organization,CDSCO 中央醫藥品標準管理機構(由印度政府衛生與家庭福利部衛生服務總局管轄)
監管概況:
注冊證書由CDSCO簽發,永久有效。
進口許可證書(表格MD-14申請)也是永久有效,但需要每5年繳費保留證書一次。

監管法規:Drugs and Cosmetics Act, 1940 and Drugs and Cosmetics Rules, 1945;Medical Devices Rules, 2017;Medical Devices (Amendment) Rules, 2020
醫療器械分類:
A類,低風險
B類,中風險
C類,中高風險
D類,最高風險
分類規則在:官網“Public Notice”部分;Medical Devices Rules, 2017, “First Schedule” 部分
生產(進口產品)商要求、產品注冊:
境外生產商首先需要指定印度境內的代理持證人,角色包含總代、注冊代理等,直接與CDSCO溝通注冊等事宜。代理持證公司具體收費(代持證書費用、進口業務費用等)自定。代理持證人必須持有有效的批發許可證(表格20B和21B / 21C)。
GMP要求:ISO 13485(需要有代理持證人遞交Plant Master File到CDSCO進行體系審核,如有必要CDSCO可要求現場審核醫療器械生產商)
特殊要求:
C、D類產品必須在印度境內進行臨床試驗,除非有認可國家/地區(歐盟、美國、日本、加拿大、澳大利亞)發出的自由銷售證明。
Where a medical device is imported from countries other than those referred to in sub-rule (3), the licence in case of Class C and Class D medical devices may be granted after its safety and effectiveness has been established through clinical investigation in India as specified under provisions of Chapter VII of these rules.

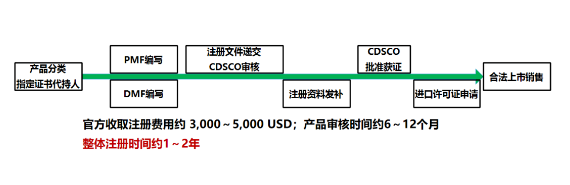
注冊流程、時間及收費情況