原則類型:體外診斷試劑 產品類型:診斷試劑 臨床科室:檢驗科管理類別:二
總三碘甲狀腺原氨酸檢測試劑注冊技術審查
指導原則
本指導原則旨在為注冊申請人對總三碘甲狀腺原氨酸檢測試劑注冊申報資料的準備和撰寫,以及技術審評部門審評注冊申報資料提供參考。
本指導原則是對總三碘甲狀腺原氨酸檢測試劑的一般要求,申請人應依據產品的具體特性確定其中內容是否適用,若不適用,需詳細闡述理由及相應的科學依據,并根據產品的具體特性對注冊申報資料的內容進行充實和細化。
本指導原則是供申請人和審評人員使用的指導性文件,不涉及注冊審批等行政事項,亦不作為法規強制執行,如有能夠滿足法規要求的其他方法,也可以采用,但應提供詳細的研究資料和驗證資料。應在遵循相關法規的前提下使用本指導原則。
本指導原則是在現行法規、標準體系以及當前認知水平下制訂的,隨著法規、標準體系的不斷完善和科學技術的不斷發展,本指導原則相關內容也將適時進行調整。
一、適用范圍
總三碘甲狀腺原氨酸檢測試劑是指利用抗原抗體反應的免疫學檢測方法對人血清、血漿中的總三碘甲狀腺原氨酸(Total Triiodothyronine,TT3)進行體外定量檢測的試劑。
本指導原則適用于以酶標記、(電)化學發光標記、(時間分辨)熒光標記等標記方法標記,以微孔板(管)、磁顆粒、微珠和塑料珠等為載體,采用競爭法定量檢測人TT3的免疫分析試劑的首次注冊申報和相關許可事項變更注冊。以膠體金標記的TT3試紙條以及用125I等放射性同位素標記的各類TT3放射免疫或免疫放射檢測試劑不適用本指導原則。
依據《體外診斷試劑注冊管理辦法》(國家食品藥品監督管理總局令第5號)《體外診斷試劑注冊管理辦法修正案》(國家食品藥品監督管理總局令第30號)和《食品藥品監管總局關于印發體外診斷試劑分類子目錄的通知》(食藥監械管〔2013〕242號),總三碘甲狀腺原氨酸檢測試劑應按照第二類醫療器械管理,分類編碼為6840。
二、注冊申報資料要求
(一)綜述資料
綜述資料主要包括產品預期用途、產品描述、有關生物安全性方面的說明、有關產品主要研究結果的總結和評價以及同類產品在國內外上市情況介紹等內容,其中同類產品上市情況介紹部分應著重從方法學、性能指標、參考區間及臨床應用情況等方面寫明申請注冊產品與目前市場上已獲批準的同類產品之間的異同。綜述資料應符合《體外診斷試劑注冊管理辦法》(國家食品藥品監督管理總局令第5號)和《關于公布體外診斷試劑注冊申報資料要求和批準證明文件格式的公告》(國家食品藥品監督管理總局公告2014年第44號)的相關要求。
1.產品預期用途及相關的臨床適應癥背景情況
1.1三碘甲狀腺原氨酸(3,5,3’-L-三碘甲狀腺原氨酸,T3)是由甲狀腺合成和分泌(占大約20%)或由甲狀腺素在5’位脫碘轉化而來(占大約80%)的一種激素,分子量為651Da,是目前已知生物活性最強的甲狀腺激素,其生物活性為甲狀腺素(T4)的3~5倍。在血液循環中,99.7%的T3與結合蛋白結合,發揮生理活性的是游離的T3(FT3)。游離T3檢測對疾病診斷的靈敏度和特異性較好,但相對總T3而言更容易受到一些疾病和藥物的干擾導致結果假性偏高或偏低,此時總T3檢測結果更能準確反映體內三碘甲狀腺原氨酸的狀態。總三碘甲狀腺原氨酸(TT3)是指血清或血漿中游離態和結合態三碘甲狀腺原氨酸的總和,在臨床上主要用于輔助診斷甲狀腺功能亢進癥(簡稱甲亢)、甲狀腺功能減低癥(簡稱甲減)及其臨床療效的評價等。
TT3在正常和病理狀態下的水平特點,不同類型疾病、不同人群(例如年齡、性別、妊娠情況等)的TT3水平差異。詳細說明測定TT3水平對相關疾病的臨床指導意義。
TT3升高見于:①甲亢,包括原發性/繼發性甲亢、T3型甲亢;②亞急性甲狀腺炎和無痛性甲狀腺炎;③促甲狀腺激素(TSH)不適當分泌綜合征。
TT3降低見于:①甲減;②甲狀腺切除術后;③應用雄激素、糖皮質激素、生長激素等藥物引起TBG降低。
1.2申請人應描述產品的預期用途、與預期用途相關的臨床適應癥背景情況,如臨床適應癥的發生率、易感人群等,相關的臨床或實驗室診斷方法等。
2.產品描述
包括產品所采用的技術原理、主要原材料的來源、質量控制及制備方法、主要生產工藝過程及關鍵控制點,質控品(如有)、校準品(如有)的制備方法、賦值過程及溯源情況。
3.有關生物安全性方面的說明
體外診斷試劑中的主要原材料,如果采用動物、病原體、人源的組織或體液等生物材料經處理或添加某些物質制備而成,需對有關傳染病(HIV、HBV、HCV等)病原體檢測予以說明,并提供相關的證明文件。其他動物源及微生物來源的材料,應當提供相應的說明文件,證明其在產品運輸、使用過程中對使用者和環境是安全的,并對上述原材料所采用的滅活等試驗方法進行說明。
4.有關產品主要研究結果的總結和評價
5.其他
包括同類產品在國內外批準上市的情況,相關產品所采用的技術方法及臨床應用情況,申請注冊產品與國內外同類產品的異同等。
6.參考文獻(如有)。
(二)主要原材料的研究資料(如需提供)
1.測定試劑所用活性材料(抗原、抗體)的制備、篩選、純化以及鑒定等詳細試驗資料。若活性材料為申請人自制,則應詳述活性材料的名稱及生物學來源,申請人對該活性材料技術指標的要求(如外觀、純度、蛋白濃度、效價等),且其生產工藝必須相對穩定,并對其工藝有相關的驗證,同時確定該活性材料作為主要原材料的依據和質量標準;若為申請人外購,則應詳述其名稱及生物學來源、供應商名稱,提交活性材料質量標準及檢驗報告,詳述申請人對該活性材料技術指標的要求以及申請人確定該活性材料作為主要原材料的依據。
其他原材料,如標記用發光物或酶、固相載體(如:酶標板、微孔板、磁珠)等,申請人應明確來源及相應的技術指標要求(如發光物的穩定性、酶的純度值及功能性實驗、固相載體的外觀、材質、吸附能力等)。
2.校準品、質控品(如有)的原料選擇、制備、定值過程及試驗資料。申請人應根據GB/T 21415—2008/ISO 17511:2003《體外診斷醫療器械 生物樣品中量的測量 校準品和控制物質賦值的計量學溯源性》提供校準品的溯源性文件,校準品應溯源至現行的國家(或國際)標準品。
(三)主要生產工藝及反應體系的研究資料(如需提供)
主要生產工藝一般應包括:工作液的配制、分裝、凍干、固相載體的包被和組裝,顯色/發光系統等的描述及確定依據等。反應體系包括:樣本采集及處理、樣本要求、樣本用量、試劑用量、反應條件、校準方法、質控方法等。
1.主要生產工藝介紹,可以流程圖方式表示,并簡要說明主要生產工藝的確定依據。
2.產品反應原理介紹。
3.樣本采集及處理,樣本要求:應充分考慮樣本的穩定性等因素,提供樣本采集處理和樣本要求的最佳條件。
4.活性材料包被/標記工藝研究:申請人應考慮如包被緩沖液(類型、pH)及其添加量、活性材料濃度、時間、穩定性等指標對產品性能的影響,通過試驗確定上述指標的最佳組合。
5.體系反應條件確定:申請人應考慮反應模式、反應時間、反應溫度、洗滌次數等條件對產品性能的影響,通過試驗確定上述條件的最佳組合。
6.體系中樣本與試劑的加樣方式及其添加量確定:申請人應考慮樣本加樣方式、加樣量以及試劑添加順序、添加量對產品檢測結果的影響,通過試驗確定最佳樣本與試劑的添加方式及其添加量。若樣本需采取稀釋或其他必要的方法進行處理后方可用于最終檢測,申請人還應對可用于樣本稀釋的基質或處理方法進行研究,通過試驗確定樣本稀釋基質或處理方法。確定反應所需其他試劑的要求(校準品、標記物、底物等)的研究資料。
7.不同適用機型的反應條件如果有差異應分別詳述。
(四)分析性能評估資料
申請人應提交產品研制階段進行的所有性能驗證的研究資料,包括具體研究方法、質控標準、實驗數據、統計分析等詳細資料。選擇不少于3批產品對分析性能指標進行研究:包括準確度、空白限、檢出限、線性、精密度(分析內精密度、批間精密度)等,性能評估時應將試劑(盒)和所選用的校準品、質控品作為一個整體進行評價,評估整個系統的性能是否符合要求。具體研究方法建議參考國外相關指南或國內有關體外診斷產品性能評估文件、行業標準等。
1.準確度
準確度的評價途徑包括:
與國家(或國際)標準品的比對研究、與國家(或國際)標準品的偏差分析、方法學比對、回收實驗等方法。(申請人可根據實際情況選擇其中一種方法進行研究,優先采用與國家(或國際)標準品的比對研究)。
1.1與國家(或國際)標準品的比對研究
用試劑盒緩沖體系將TT3國家(或國際)標準品配制成與試劑盒校準品相應的(一般應不少于5個)濃度點,試劑盒校準品與相應的國家(或國際)標準品同時進行分析測定,每點平行測定不少于2次,用log-logit或其他適當的數學模型擬合,計算兩條劑量-反應曲線的斜率和效價比,兩條劑量-反應曲線應不顯著偏離平行;以國家(或國際)標準品為對照品,試劑盒內校準品的實測值與標示值的效價比應在0.900~1.100之間。
對于沒有配備系列校準品的試劑盒,可在試劑盒規定的測量范圍內,選擇適當的緩沖體系,將國家(或國際)標準品配制2~3個濃度點,每個濃度點平行測定不少于2次,其實測值的均值與理論值之比,應在0.850~1.150之間。
1.2與國家(或國際)標準品的偏差分析
按照標準品的緩沖體系,將國家(或國際)標準品配制2~3個濃度點,各點重復檢測3次,測試結果為Xi,按式(1)計算相對偏差(Bi),相對偏差應不超過±15%。如果3次結果都符合要求,則為合格。如果≥2次結果不符合要求,即為不合格。如果有1次結果不符合要求,應重新連續測試20次,并分別按照公式(1)計算相對偏差,如果≥19次結果符合要求,即為合格。
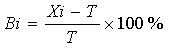
……………(1)
式中:
Bi–相對偏差;
Xi–測試結果值;
T–有證參考物質標示值
1.3方法學比對
采用參考方法或國內外普遍認為質量較好的已上市同類試劑作為參比,與擬申報試劑同時檢測同一批臨床樣本(至少40例),樣本濃度應盡量覆蓋試劑的線性范圍并均勻分布。從測定結果間的差異了解擬申報試劑與參比方法間的偏倚。如果偏倚很小或在允許的誤差范圍內,說明兩檢測系統對臨床樣本測定結果基本相符,擬申報試劑與參比方法相比,對同一份臨床樣本的醫學解釋不會產生差異結果。在實施方法學比對前,應分別對擬申報試劑和對比試劑進行初步評估,只有在確認兩者都分別符合各自相關的質量標準后方可進行比對試驗。方法學比對時應注意質量控制、樣本類型、濃度分布范圍并對結果進行合理的統計學分析。
1.4回收實驗
選擇適當濃度的常規檢測樣本,分為體積相同的3—4份,在其中2—3份樣本中加入不同濃度相同體積的待測物標準液制備待回收分析樣本(標準溶液的體積與臨床樣本的體積比應不會產生基質變化,建議標準溶液的體積不超過10%,加入標準溶液后樣品總濃度應在試劑檢測線性范圍內),制成2—3個不同濃度的待回收分析樣本,計算加入的待測物的濃度。在另一份樣本中加入同樣體積無待測物的溶劑,作為基礎樣本,測定基礎樣本的檢測濃度。用待評價系統對待回收分析樣本和基礎樣本分別進行重復3次測定,按照公式(2)計算回收率R。
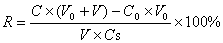
…………………………………(2)
式中:
R—回收率;
V—加入待測物標準液的體積;
V0—基礎樣本的體積;
C—樣本加入待測標準物質后的檢測濃度;
C0—基礎樣本的檢測濃度;
CS—待測物標準液的濃度。
回收率結果至少應滿足在85%~115%范圍內,同時滿足臨床需求。
2.空白限
空白限(LoB)指在聲稱概率下,空白樣本可被觀測到的最高測量結果。空白限的確定可選擇對零濃度校準品(或樣本稀釋液)進行至少20次重復檢測,計算所得信號值均值(
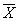
)和標準差(SD),將(

-2SD)代入劑量-反應曲線,計算出的濃度值即為空白限。空白限應不高于0.4ng/mL。
3.檢出限
檢出限(LoD)指樣本中能夠檢測出的分析物最低量。LoD一般由多個低濃度(含有分析物)樣本的檢測結果,結合LoB進行計算獲得,應根據具體產品的原理、檢測結果差異和分布,選擇合適的模型和分析方法進行計算。可參考CLSI EP17-A2的要求進行LoD的評估。
4.線性
4.1線性范圍的建立
建立試劑線性范圍所用的樣本基質應盡可能與臨床實際檢測的樣本相似,理想的樣本為分析物濃度接近預期測定上限的混合人樣本,且應充分考慮多倍稀釋對樣本基質的影響。建立一種定量測定方法的線性范圍時,需在預期測定范圍內選擇7~11個不同濃度水平。例如,將預期的線性區間加寬20%~30%,在此范圍內選擇更多的濃度水平,然后依據實驗結果逐漸減少數據點直至表現出線性關系,確定線性范圍。線性范圍的下限不高于0.8ng/mL,線性范圍的上限不低于6.0ng/mL。
超出線性范圍的樣本如需稀釋后測定,應進行相關研究,明確稀釋液類型及最大可稀釋倍數,研究過程應注意基質效應影響,必要時應提供基質效應研究有關的資料。
樣本線性可使用樣本稀釋驗證,將濃度值接近檢測范圍上限的高值樣本,按一定比例在線性范圍內稀釋不少于5個濃度點,其中低值樣本的濃度須接近線性范圍的下限。對每一濃度的樣本均重復檢測3次,計算其平均值,將測定結果平均值和稀釋比例用最小二乘法進行直線擬合,計算相關系數r,結果應不低于0.9900。(如適用)
4.2劑量反應曲線線性
劑量-反應曲線線性可使用試劑盒校準品進行驗證,用log-logit或其他適當的數學模型擬合,線性相關系數r應不低于0.9900。對于未配備校準品的試劑盒,取TT3國家標準品(或其他高濃度樣品),按照試劑盒說明書聲稱的線性范圍,配制適當的(一般不少于5個)濃度點,建立相應的劑量-反應曲線,其線性相關系數r應不低于0.9900。
5.精密度
精密度的評估應使用2~3個濃度水平的質控品進行測定,濃度宜包括參考區間上下限附近的濃度值。
一般包括分析內、批間精密度的評價。
5.1分析內精密度
在劑量-反應曲線的不同區域設置2~3個質控品,在同一分析內,每個質控品重復測定不少于8次,計算其測量結果的平均值(

)和標準差(SD),根據公式CV=SD/

×100%得出變異系數,手工操作試劑盒質控品測定結果的變異系數(CV)應不大于15.0%,全自動免疫分析系統試劑盒質控品測定結果的變異系數(CV)應不大于8.0%。
5.2批間精密度
在劑量-反應曲線的不同區域設置2~3個質控品,用不少于3個批次的產品進行獨立分析,質控品測定值變異系數(CV)應不大于20.0%。
6.質控品測定值
配備定值質控品的試劑盒,在劑量-反應曲線的不同區域的質控品(通常為2~3個),其測定結果應在試劑盒規定的范圍內。
7.分析特異性
7.1交叉反應
與易產生交叉反應的其他激素及類似物等的驗證情況,應至少驗證與總甲狀腺素(TT4)和反三碘甲狀腺原氨酸(rT3)的交叉反應情況,其中TT4濃度不低于500ng/mL,rT3濃度不低于50ng/mL,在總三碘甲狀腺原氨酸檢測試劑盒上的測定結果應不高于2.0ng/mL。
交叉反應評估的其他物質包括分析物的結構類似物、易共存的其他類似物、易產生交叉反應的其他激素等,如一碘酪氨酸、二碘酪氨酸等。
7.2干擾物質
應明確樣本中常見干擾物質對檢測結果的影響,如對脂血(甘油三酯)、黃疸(膽紅素)、溶血(血紅蛋白)、類風濕因子、異嗜性抗體等干擾因素的研究,干擾物質濃度的分布應覆蓋人體生理及病理狀態下可能出現的物質濃度,并對干擾的程度進行量化。如無法獲得含有高濃度干擾物質的樣本,可采用純品物質分別添加到健康人樣本、參考區間附近樣本、中濃度值樣本中的方式進行驗證。
藥物干擾的研究可根據需要由申請人選擇是否進行或選擇何種藥物及其濃度進行。
8.抗凝劑的影響
如果試劑盒適用樣本類型包括血漿樣本,應采用各種適用抗凝劑抗凝的血漿樣本分別與血清樣本進行對比實驗研究。方法為對比線性范圍內的同一個體的血清和血漿樣本(每種抗凝劑樣本至少30例),應包含參考區間上下限附近樣本進行檢測以驗證申報試劑對于血清和血漿樣本檢測結果的一致性。
9.其他需注意問題
9.1對于適用多個機型的產品,應提供產品說明書【適用儀器】項中所列的所有型號儀器的性能評估資料。
9.2包裝規格
如不同的包裝規格產品間存在性能差異,提交每個包裝規格產品項目評估的試驗資料及總結;如不同包裝規格之間不存在性能差異,需要提交不同包裝規格之間不存在性能差異的說明。
9.3校準品溯源及質控品賦值(如適用)
應參照GB/T 21415—2008/ISO 17511: 2003《體外診斷醫療器械 生物樣品中量的測量 校準品和控制物質賦值的計量學溯源性》的要求,提供企業(工作)校準品及試劑盒配套校準品的定值資料、不確定度資料以及其他需要提供的研究資料;提供質控品賦值資料、靶值范圍確定資料以及其他需要提供的研究資料。
(五)參考區間確定資料
提供參考區間確定所采用的樣本來源、確定方法及詳細的試驗資料。應明確參考人群的篩選標準。樣本來源應考慮不同年齡、性別、地域等因素,盡可能考慮樣本來源的多樣性、代表性。樣本例數應符合統計學要求。
(六)穩定性研究資料
穩定性研究資料主要涉及兩部分內容,即申報試劑的穩定性研究和適用樣本的穩定性研究,申報試劑的穩定性研究可參考YY/T 1579—2018《體外診斷醫療器械體外診斷試劑穩定性評價》的相關內容進行穩定性研究。
試劑的穩定性主要包括實時穩定性(有效期)和使用穩定性(如運輸穩定性、開瓶穩定性、機載穩定性等)的研究,如組分為凍干態,應有復溶穩定性研究,申請人可根據實際需要選擇合理的穩定性研究方案。穩定性研究資料應包括研究方法的確定依據、具體的實施方案、詳細的研究數據以及結論,應涵蓋產品中受穩定性影響的性能指標。對于實時穩定性研究,應提供至少三批樣品在實際儲存條件下保存至成品有效期后的研究資料。
適用樣本的穩定性主要包括室溫保存、冷藏和冷凍條件下的有效性驗證,可以在合理的溫度范圍內選擇溫度點(溫度范圍),每間隔一定的時間段即對儲存樣本進行穩定性驗證,從而確認不同類型樣本的保存穩定性。適于冷凍保存的樣本還應對凍融次數進行評價。
如產品中包含校準品和質控品,提供相應穩定性試驗研究資料。
試劑穩定性和樣本穩定性兩部分內容的研究結果應在說明書【儲存條件及有效期】和【樣本要求】兩項中分別進行詳細說明。
(七)生產及自檢記錄
提供連續三批產品生產及自檢記錄的復印件。
(八)臨床評價資料
此項目已經列入《關于新修訂免于進行臨床試驗醫療器械目錄的通告》(國家藥品監督管理局通告2018年第94號)中免于進行臨床試驗的體外診斷試劑目錄(以下簡稱“目錄”)。根據體外診斷試劑臨床評價的相關要求,申請人可按照《免于進行臨床試驗的體外診斷試劑臨床評價資料基本要求(試行)》(國家食品藥品監督管理總局通知2017年179號)要求進行臨床評價。如免臨床試驗的相關指導原則有更新,應符合相應的指導原則要求。
如不符合免于進行臨床試驗的要求,則應進行臨床試驗。通過臨床試驗方式進行臨床評價時,臨床試驗資料應符合《關于發布體外診斷試劑臨床試驗技術指導原則的通告》(國家食品藥品監督管理總局通告2014年第16號)的要求,同時研究資料的形式應符合《體外診斷試劑注冊管理辦法》(國家食品藥品監督管理總局令第5號)和《關于公布體外診斷試劑注冊申報資料要求和批準證明文件格式的公告》(國家食品藥品監督管理總局公告 2014年第44號)臨床研究資料有關的規定。
如有相應的國家法規發布或更新,按其要求執行。
(九)產品風險分析資料
申請人應考慮產品壽命周期的各個環節,從預期用途、可能的使用錯誤、與安全性有關的特征、已知及可預見的危害等方面的判定以及對患者風險的估計進行風險分析,應符合YY/T 0316—2016《醫療器械 風險管理對醫療器械的應用》的要求,企業還應根據自身產品特點確定其他危害。針對產品的各項風險,企業應采取應對措施,確保風險降到可接受的程度。
風險分析資料一般包含以下內容:
1.概述:簡要介紹風險分析資料的編制依據、適用范圍、產品描述、風險管理計劃及實施情況等;
2.風險管理人員及其職責分工:明確風險管理小組成員及職責,制定風險管理流程圖,明確風險管理活動的評審要求等;
3.風險可接受準則:明確風險可接受的準則;
4.預期用途和安全性有關特征的判定:以YY/T 0316—2016《醫療器械 風險管理對醫療器械的應用》附錄H、附錄C為基礎,判定產品預期用途和與安全性有關的特性,判定已知和可預見的危害、對患者風險的評估,并形成問題清單;
5.風險評價、風險控制和風險控制措施:對每一判定為危害的不正確結果的風險進行評價,并制定相應的風險控制方案及措施;
6.綜合剩余風險的可接受性評價:對比采取風險控制措施前后的風險情況,對剩余風險的可接受性進行評價;
7.風險控制措施驗證:對風險控制措施的有效性進行驗證分析;
8.生產和生產后監測:對產品生產和生產后的性能進行內部和外部的監測。內部監測包括生產過程控制,外部監測包括用戶投訴、不良事件、第三方性能評價等。本項內容由產品上市后補充,產品注冊時提供監測信息表格的設計內容;
9.風險管理評審結論:風險管理小組下達風險評審結論。
(十)產品技術要求
產品技術要求應符合《體外診斷試劑注冊管理辦法》(國家食品藥品監督管理總局令第5號)、《體外診斷試劑注冊申報資料要求和批準證明文件格式》和《關于發布醫療器械產品技術要求編寫指導原則的通告》(國家食品藥品監督管理總局通告2014年第9號)的相關規定。產品技術要求的性能指標應不低于國家/行業標準有關技術指標的要求。
該產品技術要求中涉及的產品適用的引用文件和主要性能指標等相關內容如下:
1.產品適用的相關標準
GB/T 191—2008 | 包裝儲運圖示標志 |
GB/T 21415—2008 | 體外診斷醫療器械 生物樣品中量的測量 校準品和控制物質賦值的計量學溯源性 |
YY/T 0316—2016 | 醫療器械 風險管理對醫療器械的應用 |
YY/T 0466.1—2016 | 醫療器械 用于醫療器械標簽、標記和提供信息的符號 第1部分:通用要求 |
YY/T 1222—2014 | 總三碘甲狀腺原氨酸定量標記免疫分析試劑盒 |
注:如標準有更新,以最新標準為準。
2.主要性能指標
2.1外觀和物理檢查
試劑盒應組分齊全,內外包裝均應完整,標簽清晰,液體試劑無滲漏,凍干組分呈疏松體,加入純化水等復溶劑后應在10min內溶解,無沉淀或絮狀物。
2.2裝量
各液體組分裝量應不少于標示裝量或規定限。
2.3空白限
可選擇重復測定零校準品(或樣本稀釋液)不少于20次,計算出反應量的均值(
![]()
)和標準方差(SD),將(
![]()
)的反應量代入劑量-反應曲線,計算出相應濃度值即為空白限。空白限應不高于0.4ng/mL。
2.4線性
在[0.8,6.0]ng/mL范圍內,用log-logit數學模型擬合或其他適當的數學模型擬合,劑量-反應曲線相關系數的絕對值(|r|)應不低于0.9900。
配備有校準品的試劑盒,校準品劑量-反應曲線線性滿足上述要求;未配備有校準品的試劑盒,取國家標準品(或其他高濃度樣品),按照試劑盒說明書聲稱的線性范圍,配制適當的(一般不少于5個)濃度點,建立相應的劑量-反應曲線,線性滿足上述要求。
注:線性范圍的下限不高于0.8ng/mL,線性范圍的上限不低于6.0ng/mL。
2.5準確度
用試劑盒緩沖體系將國家(或國際)標準品配制成與試劑盒內校準品相應的(一般不少于5個)濃度點,試劑盒內校準品與相應的國家標準品同時進行分析測定,每點平行測定不少于2次,用log-logit或其他適當的數學模型擬合,計算兩條劑量-反應曲線的斜率和效價比。要求兩條劑量-反應曲線不顯著偏離平行(t檢驗);以國家標準品為對照品,試劑盒內校準品的實測值與標示值的效價比應在0.900~1.100之間。對于沒有配備系列校準品的試劑盒,在試劑盒規定的測量范圍內,選擇適當的緩沖體系,將國家(或國際)標準品配制2~3個濃度點,每點平行測定不少于2次,其實測值的均值與理論值之比應在0.850~1.150之間。
2.6精密度
2.6.1分析內精密度
同一批次的檢測試劑對劑量-反應曲線不同區域內的2~3個濃度的質控品進行重復檢測n次(n≥8)次,計算n次測量結果的平均值(
![]()
)和標準差(SD),根據公式CV=SD/
![]()
×100%得出變異系數,手工操作試劑盒質控品測定結果的變異系數(CV)應不大于15.0%,全自動免疫分析系統試劑盒質控品測定結果的變異系數(CV)應不大于8.0%。
2.6.2批間精密度
用不少于3個批次的檢測試劑對劑量-反應曲線不同區域內的2~3個濃度的質控品各重復檢測n次(n≥8),計算3×n次測量結果的平均值(
![]()
)和標準差(SD),根據公式CV=SD/
![]()
×100%得出變異系數,變異系數(CV)應不大于20.0%。
2.7特異性
用試劑盒適當的緩沖體系,配制濃度不低于500ng/mL的三碘甲狀腺原氨酸(TT4)樣本和濃度不低于50ng/mL的反三碘甲狀腺原氨酸(rT3)樣本,在本試劑盒上的測試結果均不高于2.0ng/mL。
2.8質控品測定值
配備有定值質控品的試劑盒,在劑量-反應曲線的不同區域質控品(通常為2~3個),其測定結果應在試劑盒規定的范圍內。
2.9穩定性
2.9.1效期末穩定性:試劑盒在規定的條件下保存至有效期末,檢測試劑外觀、空白限、線性、準確度和分析內精密度、質控品測定值應符合產品技術要求。
2.9.2熱穩定性:將試劑盒在37℃條件下放置一定時間,檢測試劑外觀、空白限、線性、準確度和分析內精密度、質控品測定值應符合產品技術要求。
注1:熱穩定性不能用于推導產品有效期,除非是采用基于大量的穩定性研究數據建立的推導公式。
注2:根據產品特性可選擇2.9.1、2.9.2方法的任意組合,但所選用的方法應能驗證產品的穩定性,以保證在有效期內產品的性能符合產品技術要求。
2.9.3凍干試劑復溶后穩定性(如有):試劑盒中凍干組分按規定的條件復溶,復溶后放置到企業聲稱的復溶有效期末,檢驗試劑外觀、空白限、線性、準確度、特異性和分析內精密度應符合產品技術要求。
2.10校準品和質控品(如有)
應至少包含準確度、均一性、穩定性。凍干型校準品和質控品還應檢測批內瓶間差和復溶穩定性。
(十一)產品注冊檢驗報告
根據《關于發布體外診斷試劑注冊申報資料要求和批準證明文件格式的公告》(國家食品藥品監督管理總局公告2014年第44號)的要求,應提供符合《醫療器械監督管理條例》要求的的產品檢驗報告和產品技術要求預評價意見。
(十二)產品說明書
說明書承載了產品預期用途、樣本要求、檢驗方法、檢驗結果的解釋以及注意事項等重要信息,是指導使用者正確操作、臨床醫生針對檢驗結果給出合理醫學解釋的重要依據,因此,產品說明書是體外診斷試劑注冊申報最重要的文件之一。產品說明書的編寫應符合《醫療器械說明書和標簽管理規定》(國家食品藥品監督管理總局令第6號)和《關于發布體外診斷試劑說明書編寫指導原則的通告》(國家食品藥品監督管理總局通告2014年第17號)的要求。境外試劑的中文說明書除格式要求外,其內容應盡量保持與原文說明書的一致性,翻譯力求準確且符合中文表達習慣。產品說明書的所有內容均應與申請人提交的注冊申報資料中的相關研究結果保持一致,如某些內容引用自參考文獻,則應以規范格式對此內容進行標注,并單獨列明文獻的相關信息。
根據《醫療器械說明書和標簽管理規定》(國家食品藥品監督管理總局令第6號)和《關于發布體外診斷試劑說明書編寫指導原則的通告》(國家食品藥品監督管理總局通告2014年第17號)的要求并結合TT3本身的特點,對TT3檢測試劑說明書的重點內容進行詳細說明,以指導注冊申報人員更合理地完成說明書編制。
產品說明書內容原則上應全部使用中文進行表述;如含有國際通用或行業內普遍認可的英文縮寫,可用括號在中文后標明;對于確實無適當中文表述的詞語,可使用相應英文或其縮寫表示。
1.【產品名稱】
通用名稱應當按照《體外診斷試劑注冊管理辦法》規定的命名原則進行命名,可適當參考相關的分類目錄和/或國家標準及行業標準。
例如:總三碘甲狀腺原氨酸測定試劑盒(磁微粒化學發光法)、總三碘甲狀腺原氨酸檢測試劑盒(磁微粒化學發光法)。
注:產品名稱中不體現定性/定量、樣本類型等內容。
2.【包裝規格】
注明可測試的樣本數或裝量,如××測試/盒、××人份/盒、××mL,除國際通用計量單位外,其余內容均應采用中文進行表述。如產品有不同組分,可以寫明組分名稱。如有貨號,可增加貨號信息。
3.【預期用途】
第一段內容應說明試劑盒用于體外定量檢測人血清和/或血漿中總三碘甲狀腺原氨酸的含量。適用的樣本類型應結合實際的臨床研究情況進行確認。若用于特殊受試人群的檢測,如孕婦等,應明確說明。
第二段內容說明與預期用途相關的臨床適應癥及背景情況,說明相關的臨床或實驗室診斷方法等。
4.【檢驗原理】
詳細說明檢驗原理、方法,必要時可采用圖示方法描述。
5.【主要組成成分】
5.1說明產品包含試劑組分的名稱、數量等信息,涉及的英文縮寫應注中文表述。
5.2對于多組分試劑應明確說明不同批號試劑盒中各組分是否可以互換。
5.3如試劑盒中包含耗材,應列明耗材名稱、數量等信息,如塑料滴管、封板膜、自封袋等。
5.4對于
產品中不包含,但對該試驗必需的試劑組分,應列出此類試劑的名稱,提供稀釋或混合方法及其他相關信息。
5.5試劑盒中如包含校準品和/或質控品,除明確其組成成分及生物學來源外,校準品應明確其定值及溯源性,溯源性應寫明溯源的最高級別,包括其發布單位及編號。質控品應明確靶值范圍,如靶值范圍為批特異,可注明批特異,附單獨的靶值單,或在適當的位置注明靶值信息。
6.【儲存條件及有效期】
根據產品的實時穩定性、開瓶穩定性等穩定性研究結果,對產品的儲存條件及有效期做以下說明:
6.1說明產品的儲存條件及有效期,如:2℃~8℃、-18℃以下保存的有效期限,避免/禁止冷凍等。其他影響穩定性的條件,如:光線、濕度等也必須說明。
6.2如果打開包裝后產品或組分的穩定性不同于原包裝產品,則打開包裝后產品或組分的儲存條件及有效期也必須注明。
6.3如試劑盒各組分的穩定性不一致,則應對各組分的儲存條件和有效期分別進行描述。
6.4產品生產日期、使用期限或失效日期,見產品外包裝標簽。
7.【適用儀器】
說明可適用的儀器名稱、生產企業及型號,并提供與儀器有關的信息以便用戶能夠正確選擇使用。
7.1如適用儀器為酶標儀,需寫明對酶標儀配置的要求,至少應標明波長。
7.2除酶標儀以外的其他儀器,則需寫明具體適用儀器的型號,不能泛指某一系列儀器,并且與分析性能評估資料一致。
8.【樣本要求】
重點明確以下內容:
8.1明確本產品適用的樣本類型,血漿樣本應當說明對采血管或抗凝劑的要求。
8.2說明在樣本采集過程中,采集時間點是否受臨床癥狀、用藥情況等因素的影響,盡量減少由于樣本采集或處理不當對實驗造成的影響。
8.3明確樣本處理方法、樣本的保存條件及保存期限等,冷藏/冷凍樣本檢測前是否須恢復室溫,凍融次數的要求。
9.【檢驗方法】
詳細說明實驗操作的各個步驟。
9.1試劑配制:各試劑組分的稀釋、混合及其他必要的程序。
9.2試驗條件:溫度、每一步試驗所需的時間、測定波長、試劑用量、樣本用量、測定方法、最終反應產物的穩定性等。試驗過程中的注意事項。
9.3待測樣本的預處理方法、步驟以及注意事項。
9.4明確樣本檢測的操作步驟。
9.5校準程序:校準品的使用方法、注意事項、校準曲線的繪制方法。
9.6質量控制:質控品的使用方法、對質控結果的必要解釋以及推薦的質控周期等。建議在本部分注明:如果質控結果與預期不符,提示檢測結果不可靠,不應出具檢測報告。如質控不合格應采取糾正措施。
9.7試驗結果的計算:說明校準曲線擬合方式和結果計算方法。
10.【參考區間】
應注明常用樣本類型的正常參考區間,并簡要說明參考區間的確定方法。建議注明“由于地域、人種、性別及年齡等差異,建議各實驗室建立自己的參考區間”。
11.【檢驗結果的解釋】
對可能出現的結果進行合理的解釋。
11.1分析異常值出現的可能因素,明確說明何種情況下需要進行重復檢測,詳述在重復檢測時對待測樣本可能采取的優化條件等。
11.2超出線性范圍的樣本怎樣報告結果,如要得到準確的結果需怎樣處理,如需稀釋,應注明稀釋劑、稀釋方法、最佳或最大稀釋比例等。
11.3由于方法學或抗體特異性等原因,使用不同生產商的試劑對同一份樣本進行檢測可能會得到不同的檢測結果,因而在監測過程中,用不同試劑檢測所得結果不應直接相互比較,以免造成錯誤的醫學解釋。
12.【檢驗方法局限性】
12.1對TT3測定可能存在的限制性因素進行說明或警示。
12.2不得作為患者病情評價的唯一指標,僅作為診斷的輔助手段之一,臨床診斷應與臨床檢查、病史以及其他檢測相結合
12.3異嗜性抗體或類風濕因子等對檢測結果的影響。
12.4常見干擾物質對檢測結果的影響。
13.【產品性能指標】
對產品的主要性能指標進行描述。
至少應詳述線性、準確度、空白限、精密度(分析內精密度和批間精密度)、特異性性能指標。
14.【注意事項】
應至少包括以下內容:
14.1有關人源、動物源組分的警告,如:試劑盒內質控品、校準品或其他可能含有人源物質的組分,雖已經通過了HBsAg、HIV1/2-Ab、HCV-Ab、TP等項目的檢測,但截至目前,沒有任何一項檢測可以確保絕對安全,故仍應將這些組分作為潛在傳染源對待。
14.2建議實驗室的環境要求,如溫度、濕度、電磁環境等。
14.3對所有樣本和反應廢棄物都視為傳染源進行處理。
14.4有關實驗操作、樣本保存及處理等其他注意事項。
14.5本產品僅用于體外診斷。
14.6其他有關總三碘甲狀腺原氨酸檢測的注意事項。
15.【標識的解釋】
如有圖形或符號,請解釋其代表的意義。如沒有,本項可以缺省。
16.【參考文獻】
注明引用的參考文獻,并在說明書相應內容處標注參考文獻編號。參考文獻的格式應規范。
17.【基本信息】
根據《關于發布體外診斷試劑說明書編寫指導原則的通告》(國家食品藥品監督管理總局通告2014年第17號)的要求編寫。
18.【醫療器械注冊證編號/產品技術要求編號】
應當寫明醫療器械注冊證編號/產品技術要求編號。
19.【說明書核準日期及修改日期】
注明該產品說明書的核準日期。如曾進行過說明書的變更申請,還應該同時注明說明書批準修改的日期。
三、審查關注點
(一)技術要求中性能指標的設定及其檢驗方法是否不低于相關行業標準的要求;技術要求的格式是否符合《關于發布醫療器械產品技術要求編寫指導原則的通告》(國家食品藥品監督管理總局通告2014年第9號)的相關規定。
(二)產品說明書中的預期用途、樣本類型、儲存條件及有效期、檢驗方法、參考區間、產品性能指標等描述應分別與臨床研究資料、穩定性研究資料、主要生產工藝和反應體系研究資料、參考區間研究資料、分析性能評估資料的研究結論相一致。
(三)分析性能評估指標及其結果是否滿足產品技術要求的規定,是否滿足本指導原則中分析性能評估的要求。
(四)參考區間的確定方法是否合理,數據統計是否符合統計學的相關要求,結論是否與說明書聲稱一致。
(五)產品穩定性研究方法是否合理,穩定性結論是否與說明書聲稱一致。凍干試劑應提供復溶穩定性研究資料并在說明書儲存條件及有效期中說明。
(六)臨床評價采用的樣本類型及病例是否滿足產品聲稱的預期用途,樣本量及對比試劑的選擇、統計方法及研究結果、臨床評價報告等是否符合《免于進行臨床試驗的體外診斷試劑臨床評價資料基本要求(試行)》(國家食品藥品監督管理總局通告2017年第179號)或《關于發布體外診斷試劑臨床試驗技術指導原則的通告》(國家食品藥品監督管理總局通告2014年第16號)對相關內容的規定。
(七)產品風險分析資料的撰寫是否符合YY/T 0316—2016《醫療器械 風險管理對醫療器械的應用》的要求。
四、編寫單位
河南省食品藥品審評查驗中心





