發布時間:2023-11-29 人氣:1045 作者:
馬來西亞注冊概況;
注冊流程(根據MDA/GL/MD-01)
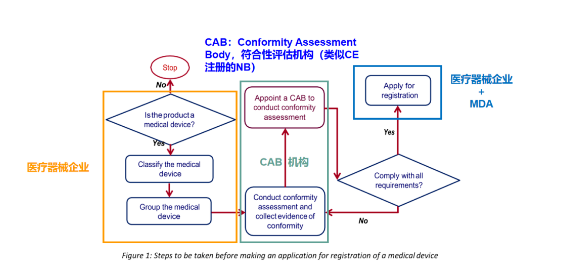
CAB的類型:產品 & 體系

產品CAB審核
根據 Conformity Assessment Procedures for Medical Device Approved by Recognised Countries: 已經在認可國家中獲得上市許可的產品,可以進行簡單產品CAB審核(證書+產品注冊文檔Verification驗證 + QMS審核的簡單CAB審核路徑,非全流程CAB審核)
如果產品沒有在認可國家中獲得上市許可,則需要進行全流程CAB審核。
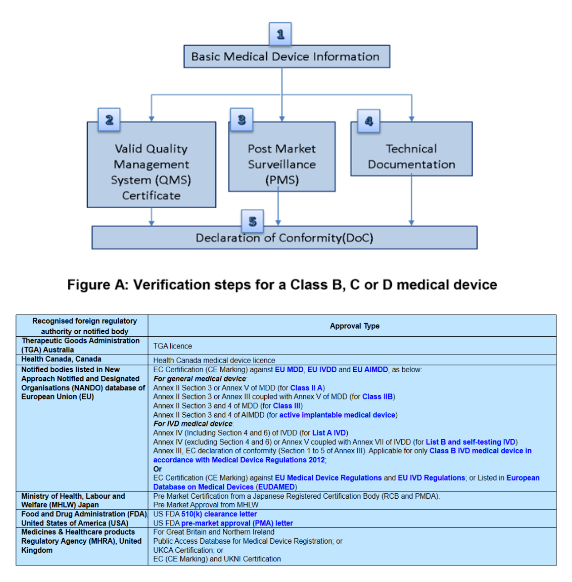
CSDT的內容要求
Executive summary 產品的概況
Relevant essential principles and rule used to demonstrate conformity 相關的基本要求符合證據
Description of medical device 器械描述
Summary of design verification and validation documents 設計驗證與確認文件
Pre-clinical studies 臨床前研究
Software validation studies 軟件確認
Medical devices containing biological material 含生物來源原料的器械
Clinical evidence 臨床證據
Medical device labelling 器械標簽
Risk analysis 風險分析
當地授權代表要求:有GDPMD證書(新申請的當地授權代表的GDPMD審核費用依據當地CAB機構制定各有不同;GDPMD現場審核排期到完成流程約1~2個月)、向MDA申請了Establishment License(授權代表MDA EL證官方收費:4000+250 RM)(當地授權代表收費視具體情況而定)
注冊時間、收費情況
MDA審核時間視情況而定,約1~6個月;B類產品收費:1000+250 RM;C類產品收費:2000+500 RM;D類產品收費:3000+750 RM
總體注冊時間約1~1.5年





