發(fā)布時(shí)間:2024-07-31 人氣:1249 作者:
在全球醫(yī)療器械領(lǐng)域,印度尼西亞作為東南亞地區(qū)的重要市場,對醫(yī)療器械制造商而言是一個(gè)不可忽視的機(jī)遇。本指南將為醫(yī)療器械制造商提供詳盡的印度尼西亞市場準(zhǔn)入策略,確保產(chǎn)品合規(guī)并順利進(jìn)入市場。
監(jiān)管機(jī)構(gòu)
印尼的醫(yī)療器械由印度尼西亞共和國衛(wèi)生部(MOH)下屬--國家藥品和食品控制局(NADFC)監(jiān)管。
主要法規(guī)
醫(yī)療器械法規(guī)(Regulation No. 62 of 2017)
參考法規(guī)
東盟醫(yī)療器械指令(ASEAN Medical Device Directive)
醫(yī)療器械風(fēng)險(xiǎn)分類
根據(jù)風(fēng)險(xiǎn)等級,醫(yī)療器械/IVD分為以下幾類:
Class A:低風(fēng)險(xiǎn)
Class B:低到中風(fēng)險(xiǎn)
Class C:中到高風(fēng)險(xiǎn)
Class D:高風(fēng)險(xiǎn)
官方費(fèi)用
印度尼西亞的注冊費(fèi)從A類的約115美元到D類的約340美元不等。
審批時(shí)間
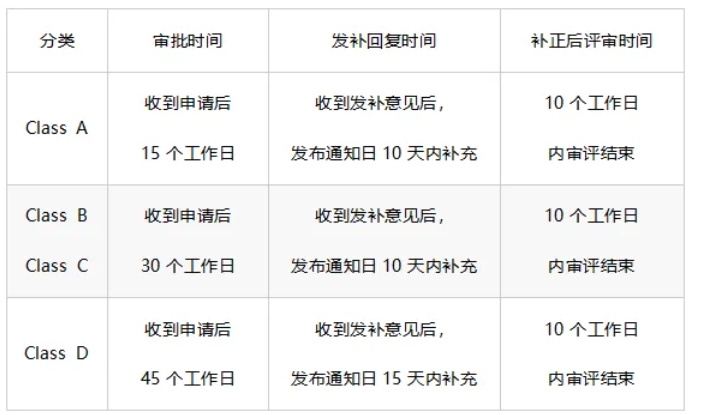
申請資料
申請表
生產(chǎn)許可/進(jìn)口許可證(申請人)
授權(quán)書
FSC
ISO13485
說明書、標(biāo)簽
風(fēng)險(xiǎn)管理
……
注冊申請流程
通過印度尼西亞醫(yī)療器械集中網(wǎng)上申請系統(tǒng)提交,簡化注冊過程。
注冊證有效期
注冊成功后,醫(yī)療器械注冊證書有效期最長為5年。
授權(quán)書的有效期最短為2年,最長為5年。該有效期的持續(xù)時(shí)間也將決定醫(yī)療器械注冊證書的有效期。
語言要求
通常情況下,注冊資料僅需以英文提供,但若產(chǎn)品的使用對象是公眾,部分文件可能需要同時(shí)以印度尼西亞語提供。
注冊資格
任何希望將產(chǎn)品進(jìn)口到印度尼西亞的公司都必須首先通過在線單一提交(OSS)系統(tǒng)進(jìn)行注冊,以獲得作為基本進(jìn)口許可證的商業(yè)識別號(NIB)。
??請注意,只有印尼當(dāng)?shù)毓静拍埽ㄍㄟ^OSS)申請NIB和醫(yī)療器械經(jīng)銷許可證IDAK(Izin Distribusi Alat Kesehatan),從而注冊和進(jìn)口醫(yī)療器械。
外國制造商必須在印尼指定一位授權(quán)代表(當(dāng)?shù)貙?shí)體公司,且擁有印尼衛(wèi)生部頒發(fā)的醫(yī)療器械經(jīng)銷商許可證);
同類產(chǎn)品只能指定一位授權(quán)代表,不得為同一設(shè)備任命多名國內(nèi)代表;
外國制造商必須簽發(fā)一份公司信箋上的授權(quán)書(LoA),由公司高管簽字并蓋章,授權(quán)國內(nèi)代表注冊醫(yī)療器械。且授權(quán)書LoA必須由當(dāng)?shù)赜∧岽笫桂^認(rèn)證。
證書轉(zhuǎn)讓
產(chǎn)品許可證,經(jīng)新舊代理雙方同意,可以從一個(gè)授權(quán)代表轉(zhuǎn)移到另一個(gè),確保業(yè)務(wù)連續(xù)性和合規(guī)性。如果對方不配合,新的申請需等6個(gè)月再提交。
醫(yī)療器械注冊流程概述
1. 確定產(chǎn)品是否屬于醫(yī)療器械及風(fēng)險(xiǎn)分類。
2. 指定印度尼西亞法定代表。
3. 準(zhǔn)備注冊文件。
4. 提交注冊文件至申報(bào)系統(tǒng)。
5. 獲取醫(yī)療器械注冊證書。
6. 合法進(jìn)入印度尼西亞市場銷售。





