(一)已按照有關規定取得企業工商登記 。
(二)已確定申報產品為第二類醫療器械,已編制完成擬申請產品的醫療器械產品技術要求,并已通過預評價
(三)已具備擬注冊產品的生產能力;已按照《醫療器械生產質量管理規范》的要求建立醫療器械生產質量管理體系 。
(四)辦理醫療器械注冊申請的人員具有相應的專業知識,熟悉醫療器械注冊管理的法規、規章和有關的技術要求。
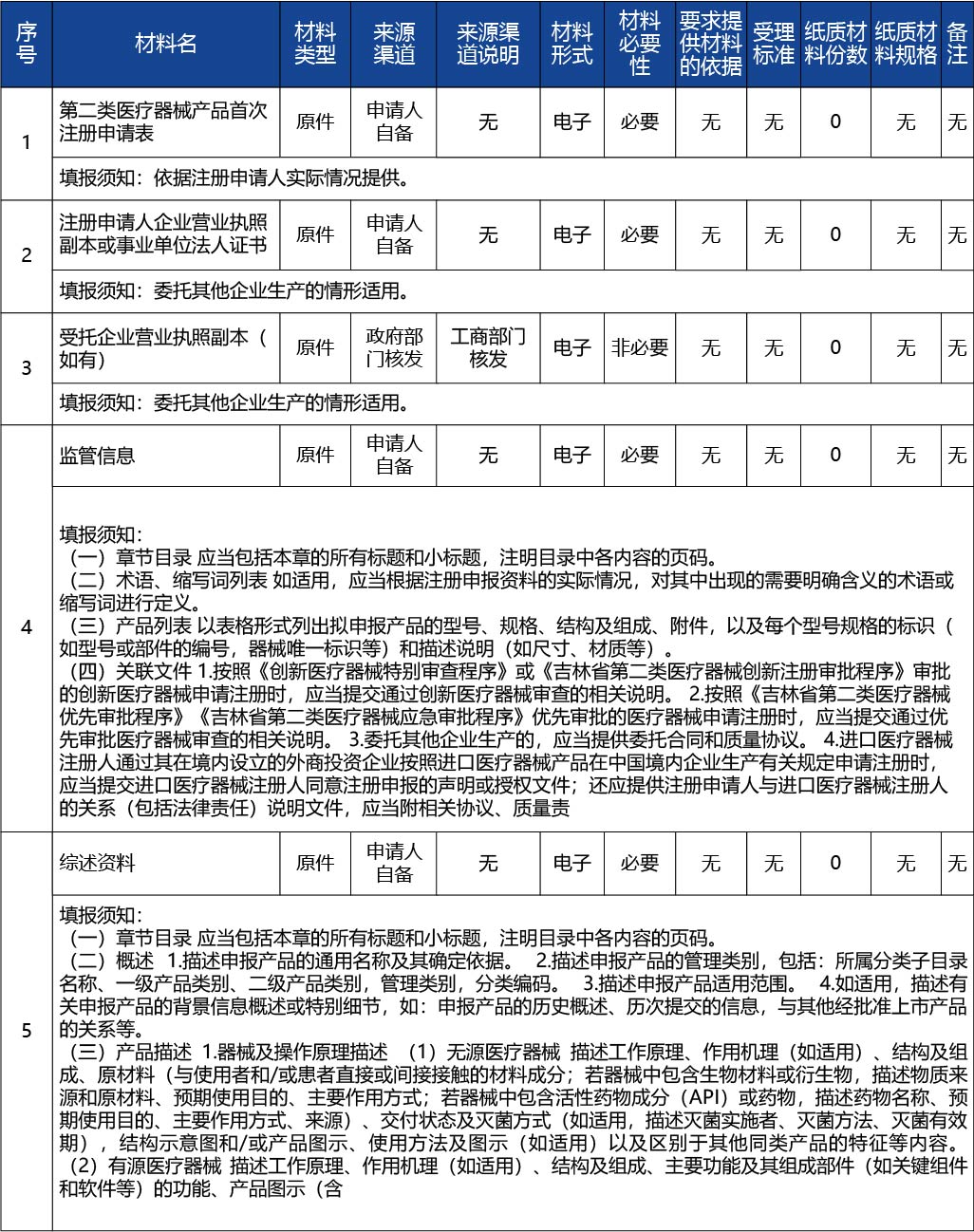
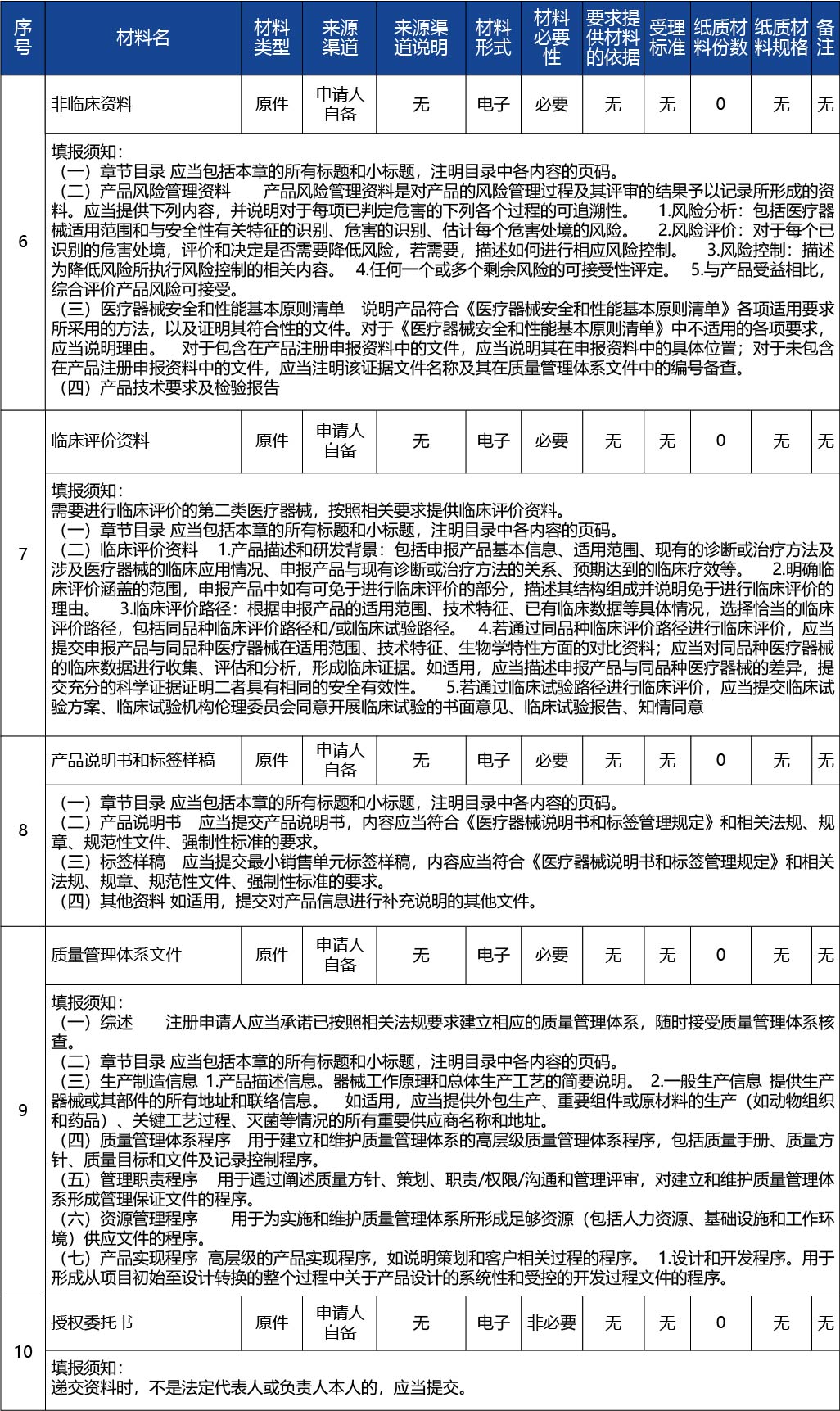
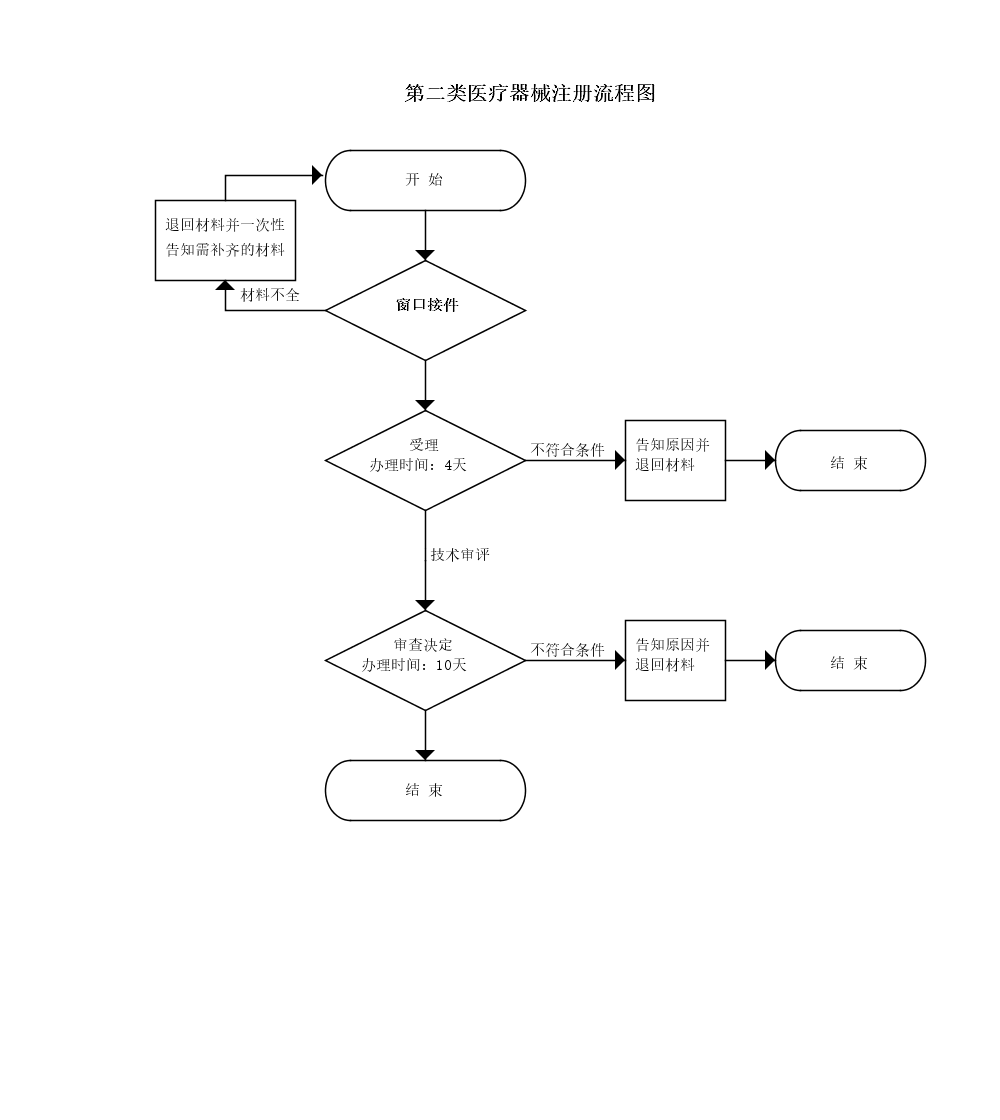
《醫療器械監督管理條例》(2000年1月4日國務院令第276號,2014年3月7日予以修改)第十一條:申請第二類醫療器械產品注冊,注冊申請人應當向所在地省、自治區、直轄市人民政府食品藥品監督管理部門提交注冊申請資料。……
不收費
行業標準提高修改產品技術要求是否屬于許可事項變更,是否收費?
答:行業標準提高企業修改相應技術要求不屬于許可事項變更,變更也不收費。
問注冊資料格式和內容能否詳細說明?
答:詳細的填寫說明請參照《關于公布醫療器械注冊申報資料要求和批準證明文件格式的公告》附件4(國家食品藥品監督管理總局2014年第43號公告)執行





