
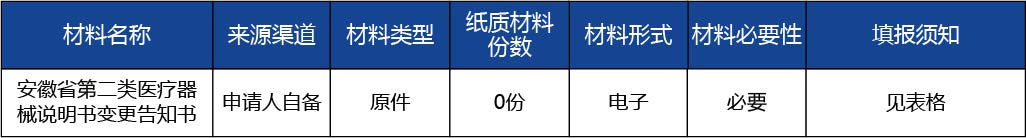
1.申報說明書產品已確定為第二類醫療器械,注冊申請人為安徽省省內企業;
2.按照有關規定取得企業營業執照和組織機構代碼證; 3.說明書已經藥品監督管理部門注冊審查;
4.說明書變更不涉及注冊證或技術要求變化;
5.辦理醫療器械注冊申請的人員具有相應的專業知識,熟悉醫療器械注冊管理的法規、規章和有關的技術要求。
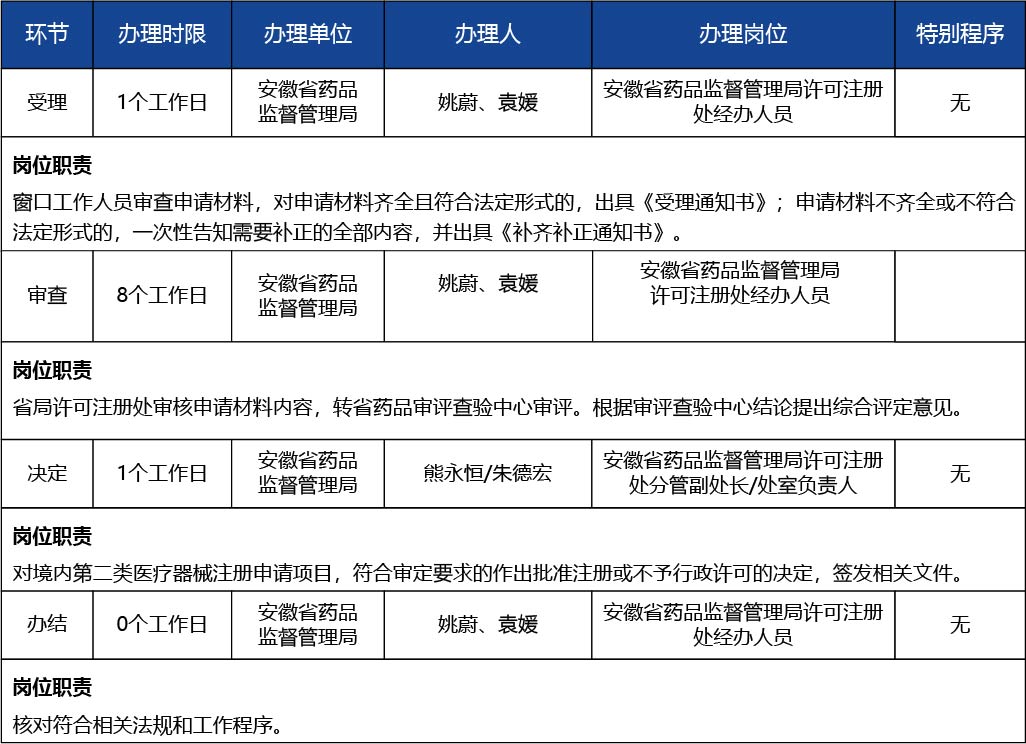
申請人備齊申請材料后,通過安徽省食品藥品監督管理局行政審批網上服務系統上傳申請材料,然后省政務服務中心藥品監管局窗口提交申請材料,窗口工作人員審查申請材料,對申請材料齊全且符合法定形式的,出具《受理通知書》(即辦件不需要);申請材料不齊全或不符合法定形式,網上或當場一次性告知需要補正的全部內容。當場受理的,申請人決定郵寄送達或自行到窗口領取,需郵寄送達的,申請人應使用正楷字書寫清楚郵寄地址、單位、收件人、電話等信息。
1.《醫療器械監督管理條例》(國務院令第739號)第三十九條 醫療器械應當有說明書、標簽。說明書、標簽的內容應當與經注冊或者備案的相關內容一致,確保真實、準確。
2.《醫療器械說明書和標簽管理規定》(國家食品藥品監督管理總局2014年第6號令)第十六條:經食品藥品監督管理部門注冊審查的醫療器械說明書的內容不得擅自更改。已注冊的醫療器械發生注冊變更的,申請人應當在取得變更文件后,依據變更文件自行修改說明書和標簽。說明書的其他內容發生變化的,應當向醫療器械注冊的審批部門書面告知,并提交說明書更改情況對比說明等相關文件。審批部門自收到書面告知之日起20個工作日內未發出不予同意通知件的,說明書更改生效。
不收費






