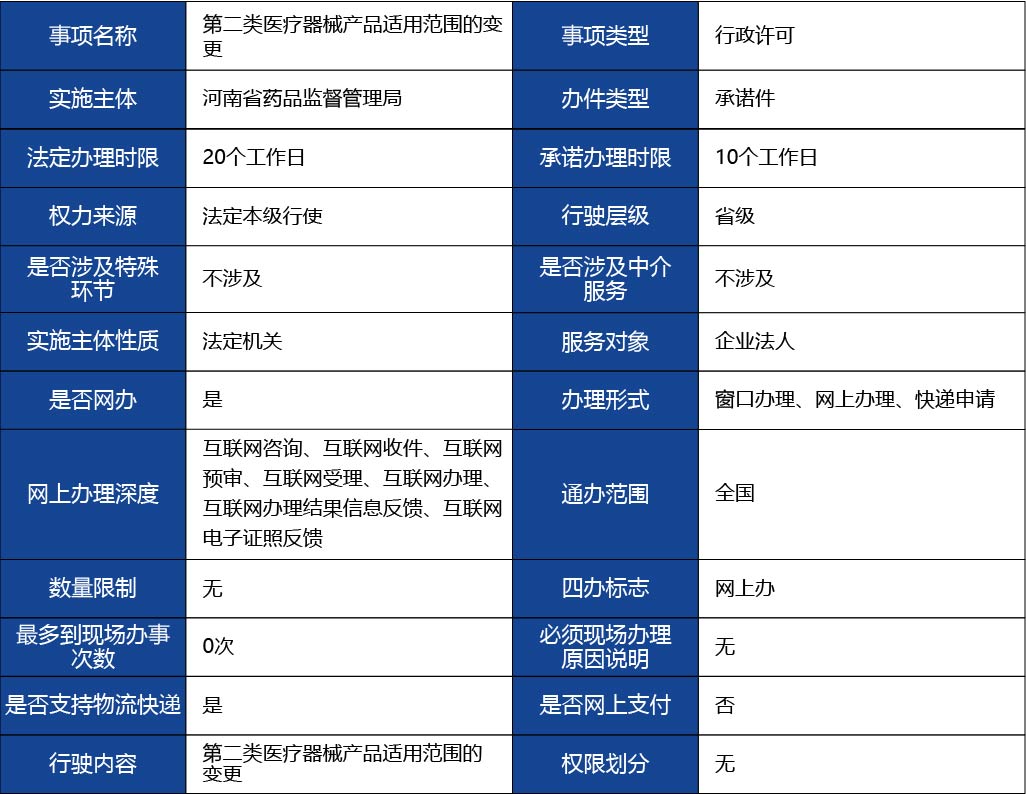
第二類醫療器械注冊證及附件載明的產品適用范圍內容發生變化的。
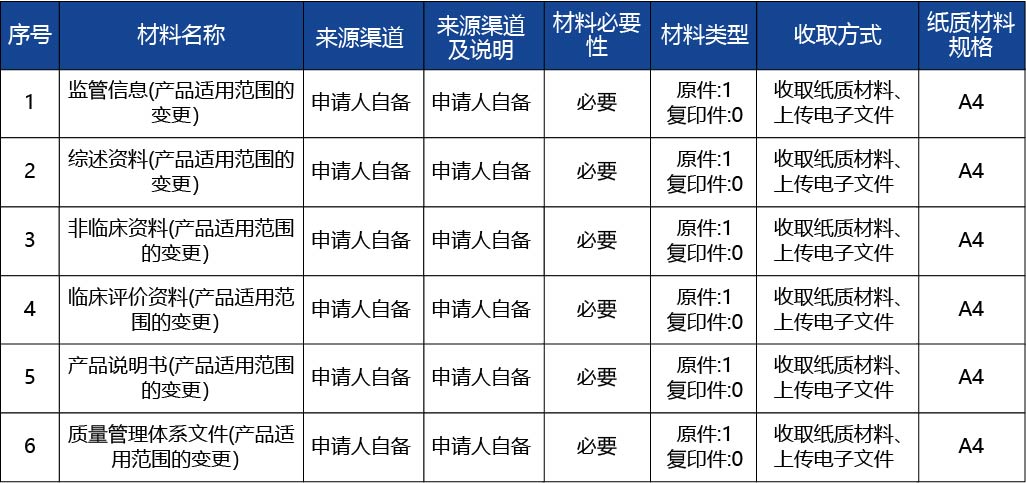
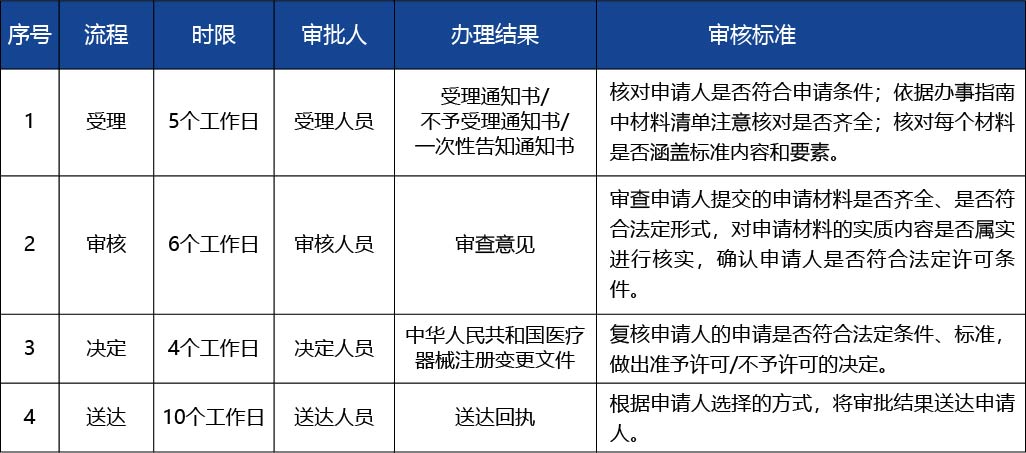
審批結果

1、《醫療器械監督管理條例》(中華人民共和國國務院令第739號)第十三條:“……,第二類、第三類醫療器械實行產品注冊管理”;第十六條:“申請第二類醫療器械產品注冊,注冊申請人應當向所在地省、自治區、直轄市人民政府藥品監督管理部門提交注冊申請資料。……”。第二十一條:“已注冊的第二類、第三類醫療器械產品,其設計、原材料、生產工藝、適用范圍、使用方法等發生實質性變化,有可能影響該醫療器械安全、有效的,注冊人應當向原注冊部門申請辦理變更注冊手續;……”
2、《醫療器械注冊與備案管理辦法》(國家市場監督管理總局令第47號)第八條:“……第二類、第三類醫療器械實行注冊管理。……境內第二類醫療器械由省、自治區、直轄市藥品監督管理部門審查,批準后發給醫療器械注冊證。……”第七十九條:“已注冊的第二類、第三類醫療器械產品,其設計、原材料、生產工藝、適用范圍、使用方法等發生實質性變化,有可能影響該醫療器械安全、有效的,注冊人應當向原注冊部門申請辦理變更注冊手續;.... 注冊證載明的產品名稱、型號、規格、結構及組成、適用范圍、產品技術要求、進口醫療器械生產地址等,屬于欠款規定的需要辦理變更注冊的事項。……”
不收費





