1.企業注冊地在廣東省內; 2.符合食藥監辦械注〔2015〕511號文中第四條要求,且能提供食藥監辦械注〔2015〕511號文中第五條材料的。
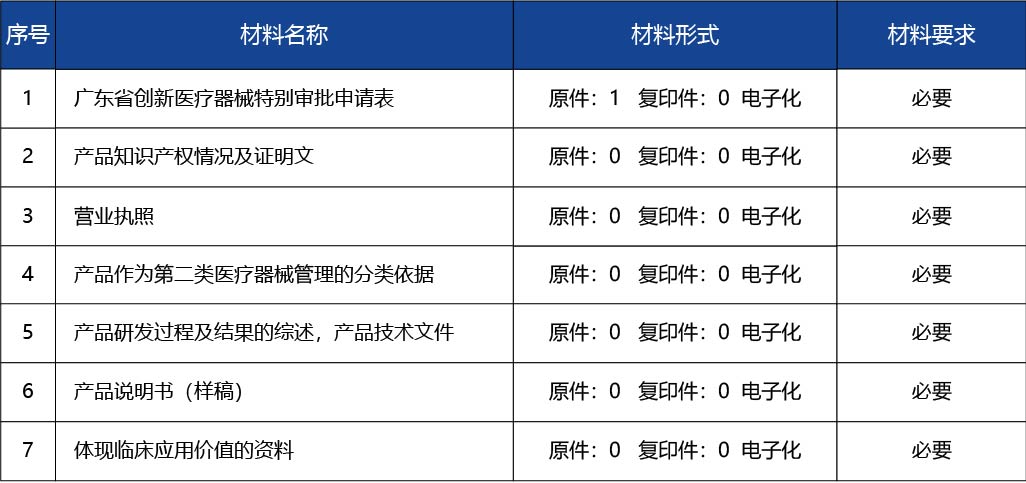
省食品藥品監督管理局對同時符合下列情形的醫療器械按本程序實施特別審批: (一)申報產品為第二類醫療器械,申請人屬于我省轄區,申報產品擬由申請人生產。 (二)申報產品擁有如下知識產權或獲獎證明之一: 1.國家級發明獎、科技進步獎; 2.省級科技進步獎二等獎以上; 3.市級科技進步獎一等獎; 4.核心技術發明專利; 5.實用新型專利(與臨床應用相關)。 (三)申報產品具有顯著的臨床應用價值,產品技術為國內領先,或可填補省內該品種醫療器械的空白,或可替代同類進口產品。 (四)申請人已完成申報產品的前期研究并具有基本定型產品,研究過程真實和受控,研究數據完整和可溯源。
不收費(廣東省藥監局)





