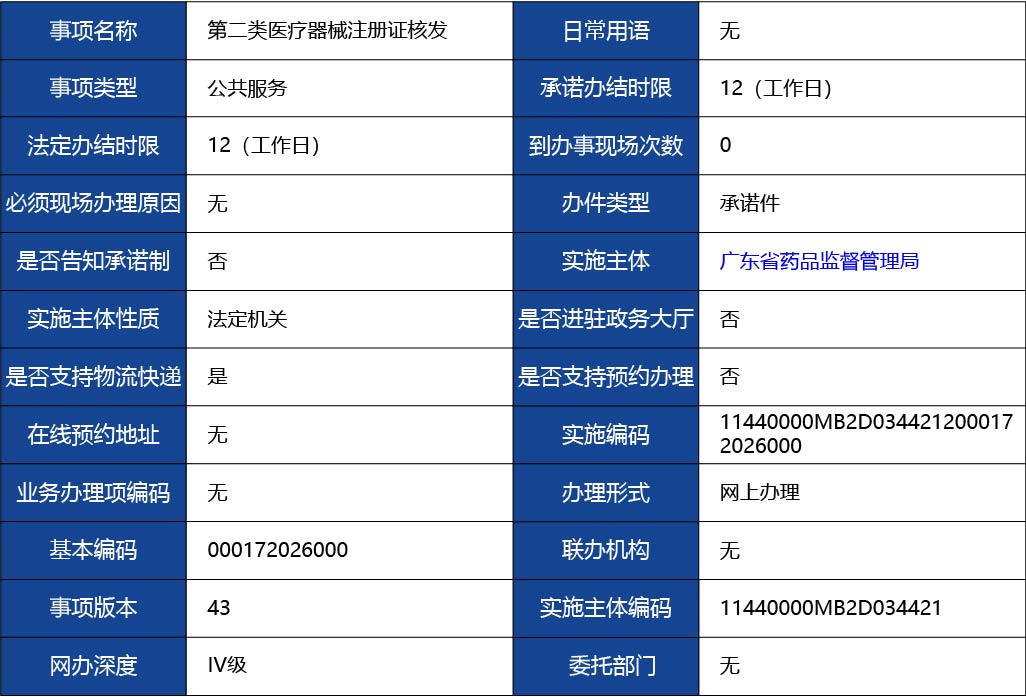
1、申報注冊的產品已經列入《總局關于發布醫療器械分類目錄的公告》(2017年第104號)的附件《醫療器械分類目錄》,且管理類別為第二類。(注:對新研制的尚未列入分類目錄的醫療器械,申請人可以直接向國家食品藥品監督管理總局申請第三類醫療器械產品注冊,也可以依據分類規則判斷產品類別并向國家食品藥品監督管理總局申請類別確認后,申請產品注冊或者辦理產品備案。)
2、申請人應當是在廣東省轄區范圍依法進行登記的企業(醫療器械注冊人制度試點申請人要求另行規定)。
3、申請人建立與產品研制、生產有關的質量管理體系,并保持有效運行。申請注冊時樣品不得委托其他企業生產,按照創新醫療器械特別審批程序審批的或符合醫療器械注冊人制度試點要求的產品除外。
4、辦理醫療器械注冊事務的人員應當具有相應的專業知識,熟悉醫療器械注冊或者備案管理的法律、法規、規章和技術要求,如:《醫療器械監督管理條例》、《醫療器械注冊管理辦法》、《醫療器械分類規則》、《關于進一步做好醫療器械產品分類界定工作的通知》、《關于發布醫療器械產品技術要求編寫指導原則的通告》、《醫療器械臨床試驗規定》、《醫療器械臨床評價技術指導原則》、《醫療器械說明書和標簽管理規定》、食品藥品監管總局關于實施《醫療器械注冊管理辦法》和《體外診斷試劑注冊管理辦法》有關事項的通知、《關于公布醫療器械注冊申報資料要求和批準證明文件格式的公告》等。
5、申請人申請注冊,應當遵循醫療器械安全有效基本要求,保證研制過程規范,所有數據真實、完整和可溯源。
6、申請注冊的資料應當使用中文。根據外文資料翻譯的,應當同時提供原文。引用未公開發表的文獻資料時,應當提供資料所有者許可使用的證明文件。申請人對資料的真實性負責。
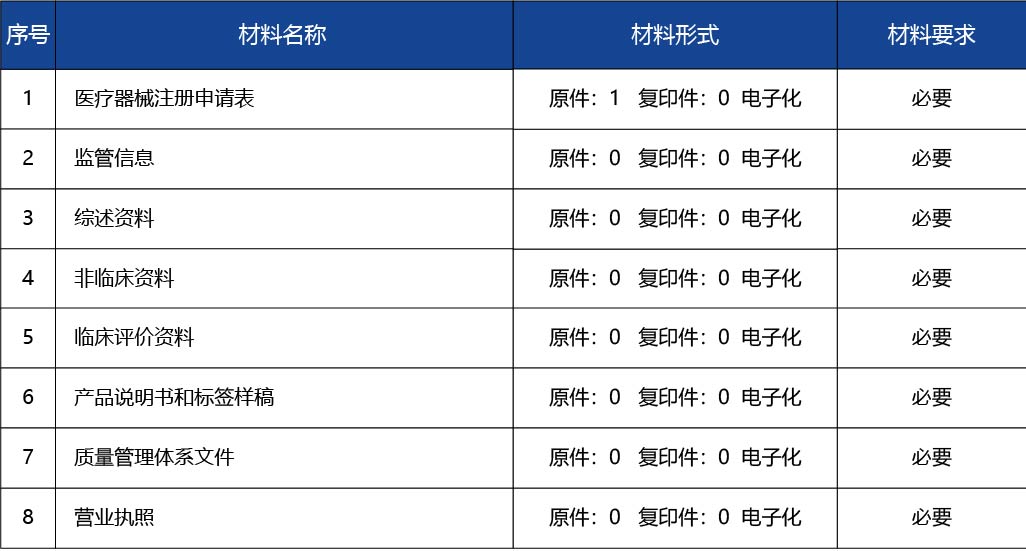
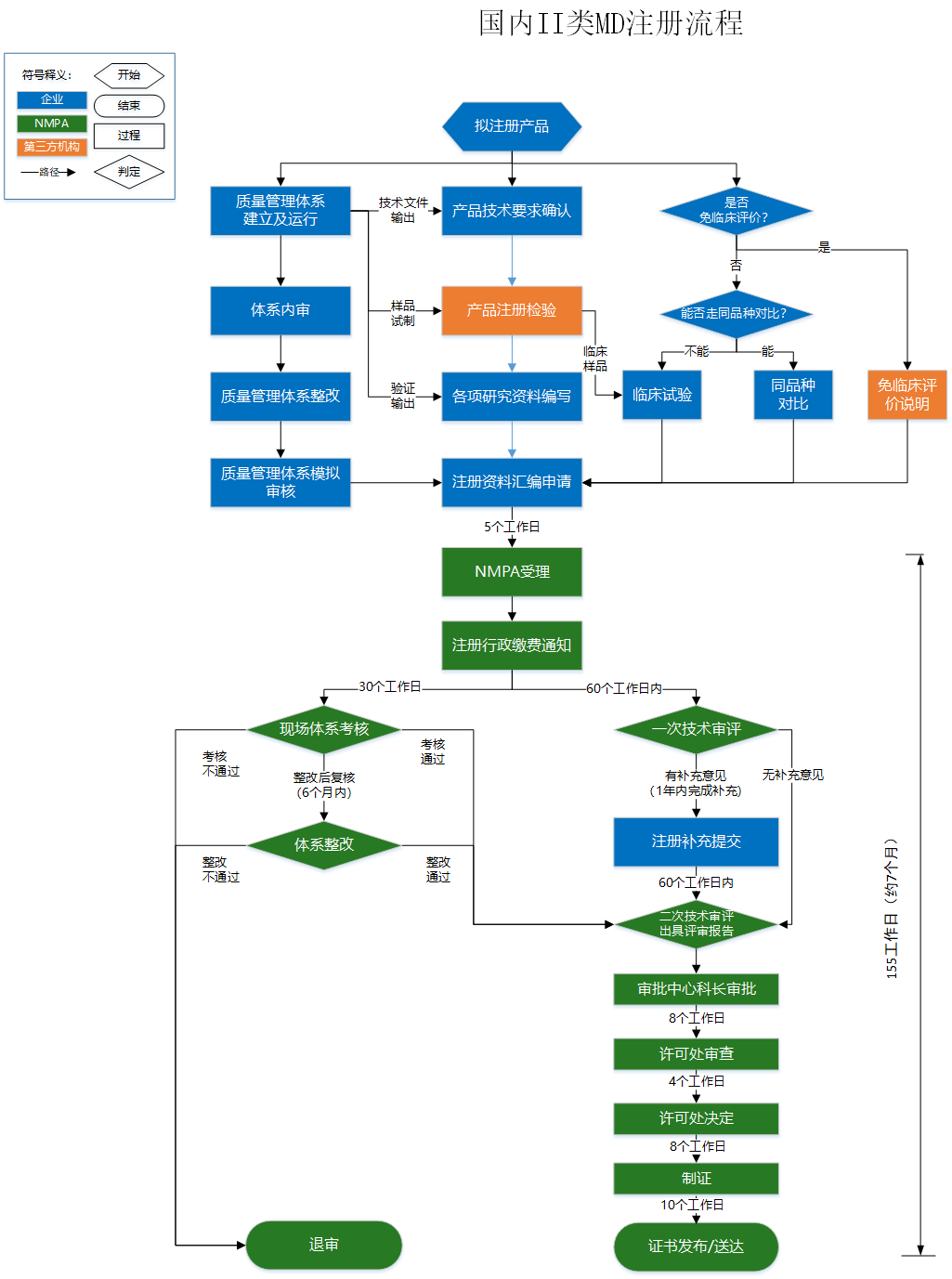
受理注冊申請的藥品監督管理部門應當自收到審評意見之日起20個工作日內作出決定。對符合條件的,準予注冊并發給醫療器械注冊證;對不符合條件的,不予注冊并書面說明理由。 受理注冊申請的藥品監督管理部門應當自醫療器械準予注冊之日起5個工作日內,通過國務院藥品監督管理部門在線政務服務平臺向社會公布注冊有關信息。

符合法定條件的,申請人有權取得本行政許可決定。申請人對本行政許可事項的辦理結果有異議的,有權依法申請行政復議或提起行政訴訟。申請人享有知情權,實施機關應當將本行政許可事項的辦理依據、條件、時限、流程及需求告知。 申請人在辦理本事項過程中,享有咨詢、辦理進程查詢、投訴的權利。
申請人應按照法規提交申請材料。申請人應對其申請材料實質內容的真實性負責。申請人應積極配合實施機關辦理本事項的相關工作,包括按要求補齊補正材料。申請人應具有相應的專業知識,熟悉醫療器械注冊管理的法律、法規、規章和技術要求。





