

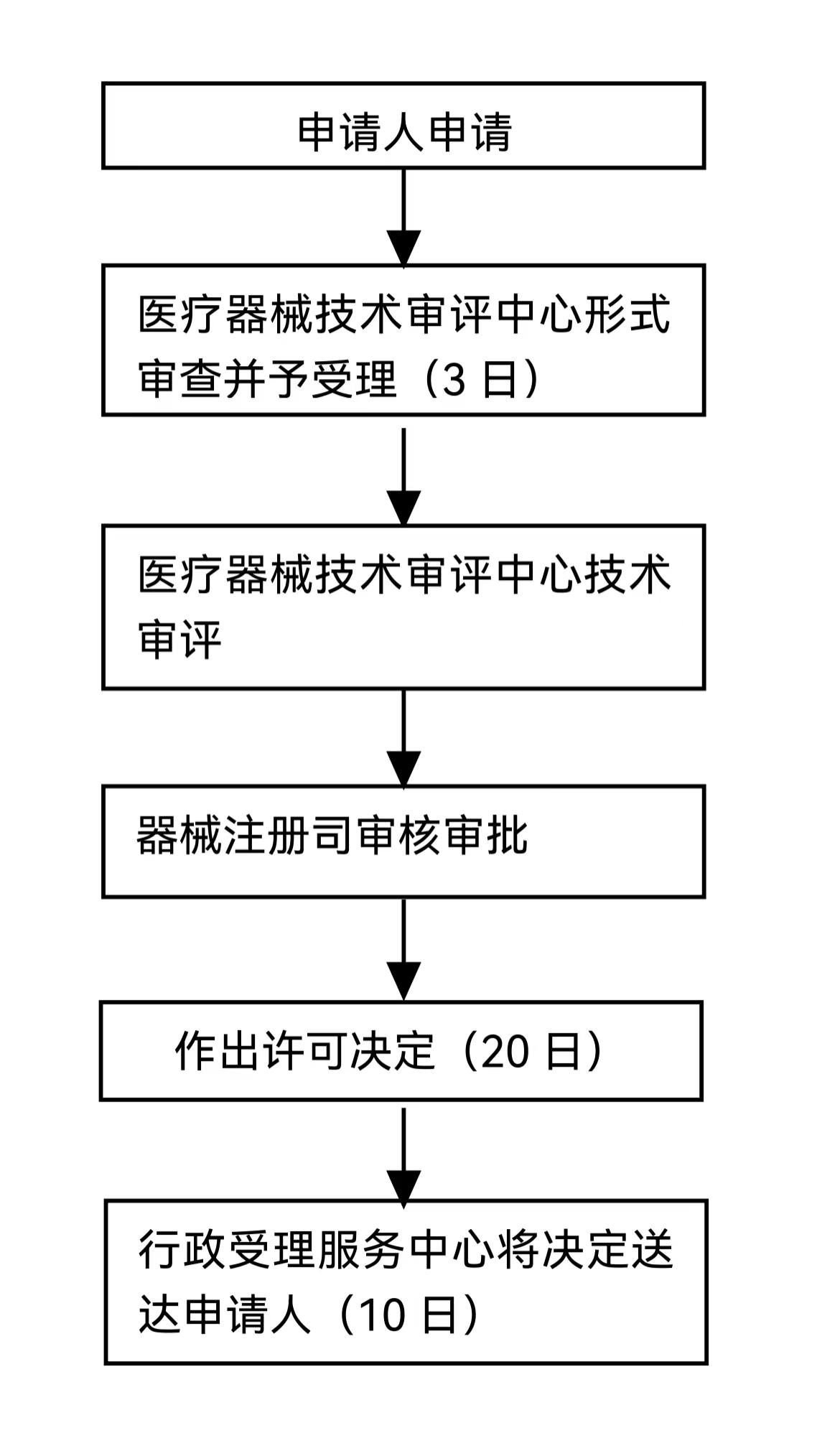
(1)申請人申請;
(2)國家藥品監督管理局受理/不予受理;
(3)技術審評機構審評;
(4)國家藥品監督管理局同意/不予同意(必要時,組織聽證)。
對于第三類高風險醫療器械臨床試驗審批決定由國家藥品監督管理局醫療器械技術審評中心以國家藥品監督管理局名義作出。
《醫療器械監督管理條例》第二十七條 第三類醫療器械臨床試驗對人體具有較高風險的,應當經國務院藥品監督管理部門批準。國務院藥品監督管理部門審批臨床試驗,應當對擬承擔醫療器械臨床試驗的機構的設備、專業人員等條件,該醫療器械的風險程度,臨床試驗實施方案。

臨床試驗申請人如何獲知申請是否通過?
答: 依據《醫療器械注冊與備案管理辦法》第四十條,由國家局器審中心網站通知申請人。





