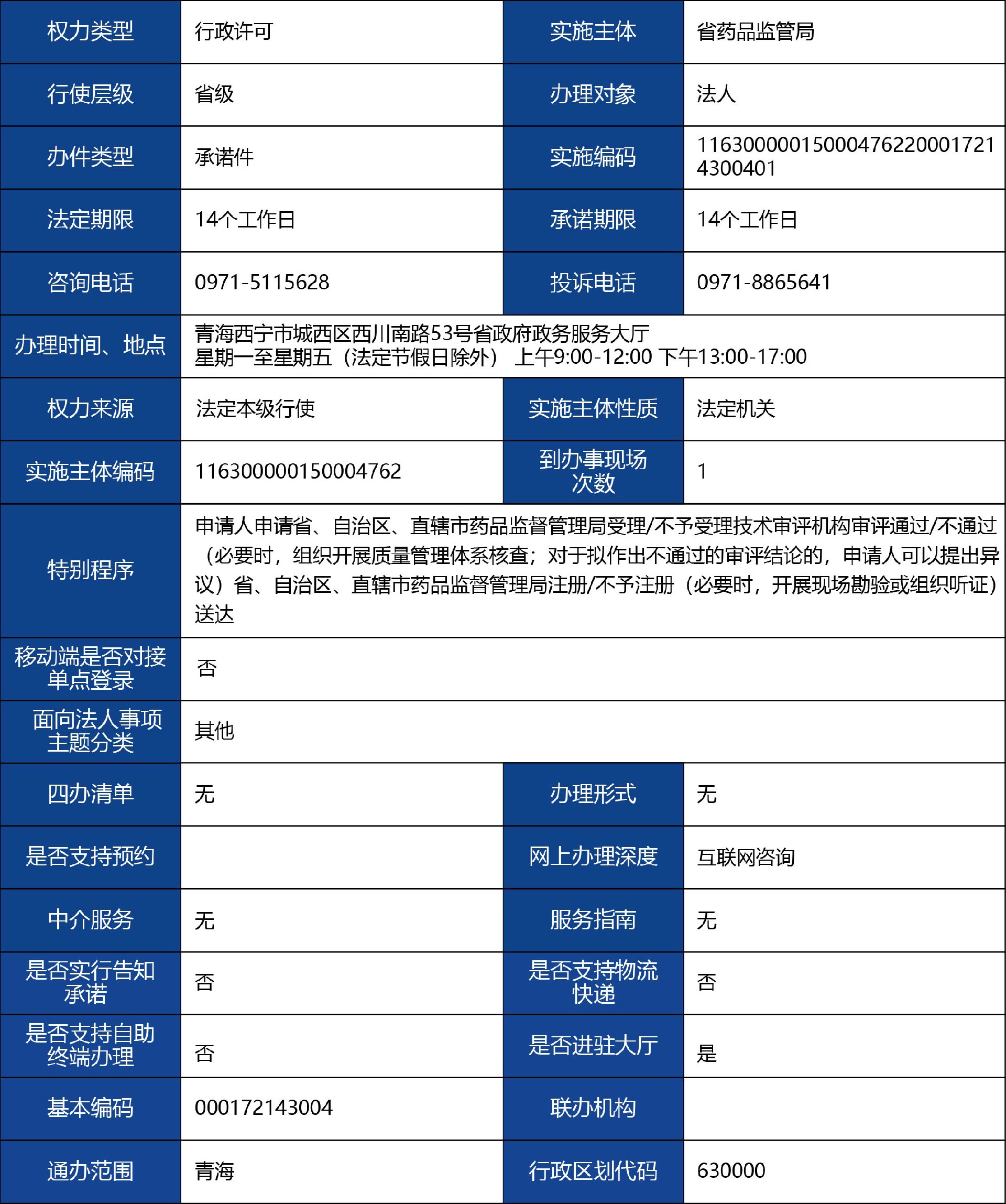
第十四條 第一類醫療器械產品備案和申請第二類、第三類醫療器械產品注冊,應當提交下列資料: (一)產品風險分析資料; (二)產品技術要求; (三)產品檢驗報告; (四)臨床評價資料; (五)產品說明書以及標簽樣稿; (六)與產品研制、生產有關的質量管理體系文件; (七)證明產品安全、有效所需的其他資料。 產品檢驗報告應當符合國務院藥品監督管理部門的要求,可以是醫療器械注冊申請人、備案人的自檢報告,也可以是委托有資質的醫療器械檢驗機構出具的檢驗報告。 符合本條例第二十四條規定的免于進行臨床評價情形的,可以免于提交臨床評價資料。 醫療器械注冊申請人、備案人應當確保提交的資料合法、真實、準確、完整和可追溯。
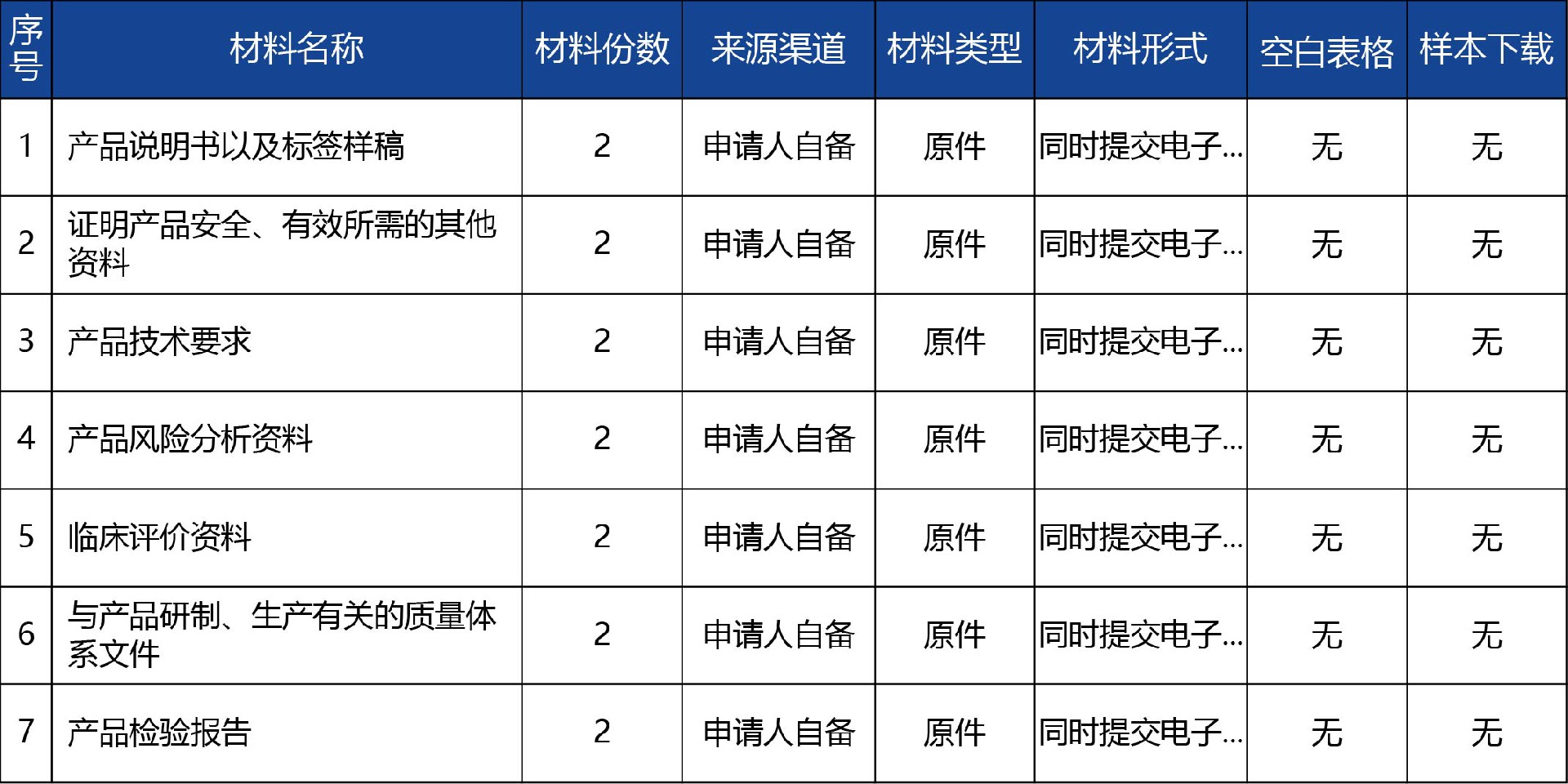
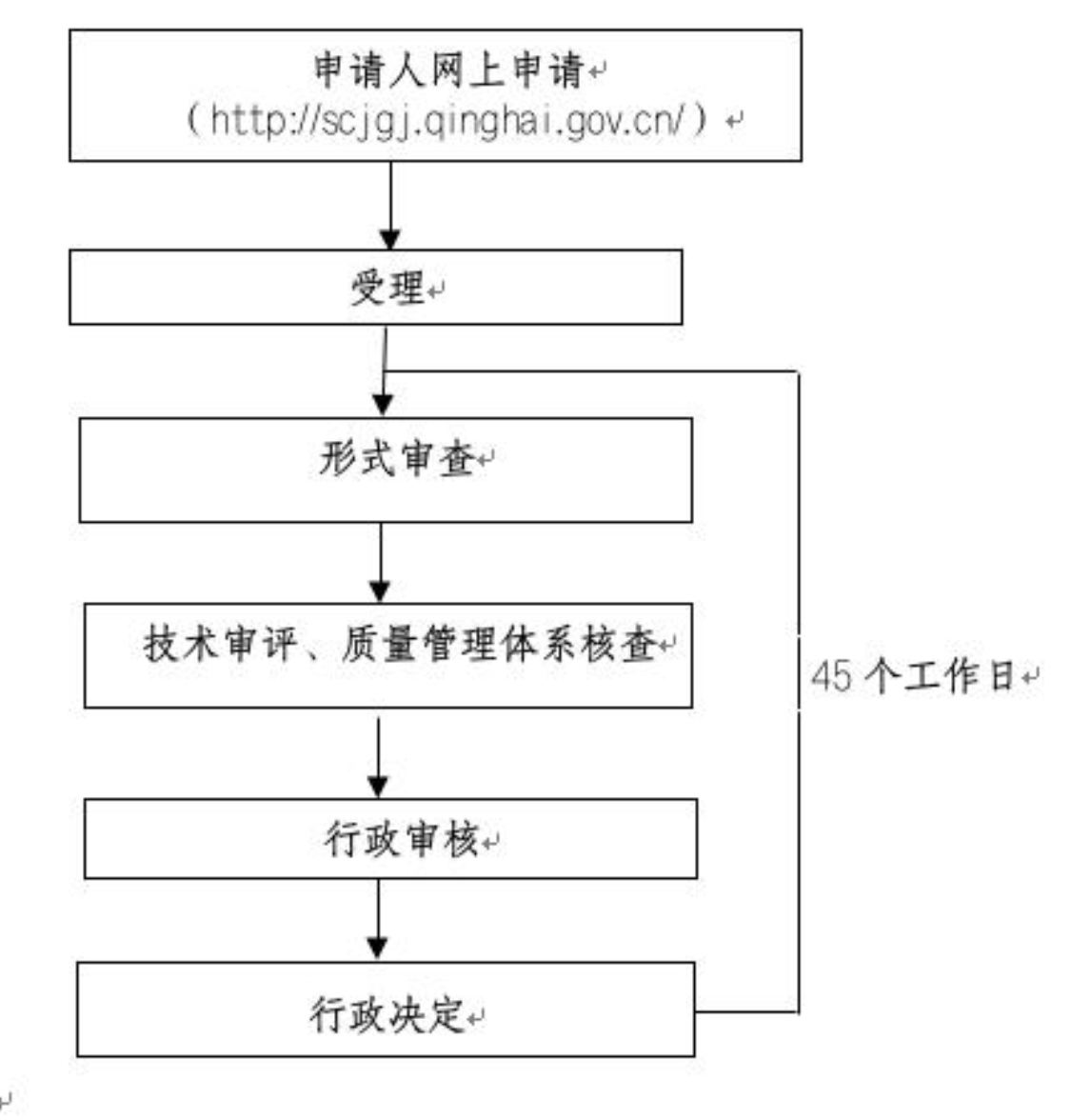
《醫療器械監督管理條例》第十六條:申請第二類醫療器械產品注冊,注冊申請人應當向所在地省、自治區、直轄市人民政府藥品監督管理部門提交注冊申請資料。申請第三類醫療器械產品注冊,注冊申請人應當向國務院藥品監督管理部門提交注冊申請資料。向我國境內出口第二類、第三類醫療器械的境外注冊申請人,由其指定的我國境內企業法人向國務院藥品監督管理部門提交注冊申請資料和注冊申請人所在國(地區)主管部門準許該醫療器械上市銷售的證明文件…… 第二十一條:已注冊的第二類、第三類醫療器械產品,其設計、原材料、生產工藝、適用范圍、使用方法等發生實質性變化,有可能影響該醫療器械安全、有效的,注冊人應當向原注冊部門申請辦理變更注冊手續;發生其他變化的,應當按照國務院藥品監督管理部門的規定備案或者報告。 第二十二條:醫療器械注冊證有效期為5年。有效期屆滿需要延續注冊的,應當在有效期屆滿6個月前向原注冊部門提出延續注冊的申請……
無
無





